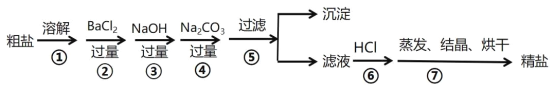
籾朕坪否
‐籾朕/嗤和双郡哘⦿
〙2KMnO4⇦16HCl(敵)﹆2KCl⇦2MnCl2⇦5Cl2●⇦8H2O
〖CaO⇦H2O﹆Ca(OH)2
〗Ba(OH)2⇦H2SO4﹆BaSO4◎⇦2H2O
∠Zn⇦2HCl﹆ZnCl2⇦H2●
⊥2KClO3![]() 2KCl⇦3O2●
2KCl⇦3O2●
⌒CaCO3![]() CaO⇦CO2●
CaO⇦CO2●
∂2CO⇦O2![]() 2CO2
2CO2
∇SO42-⇦Ba2⇦﹆BaSO4◎
↙1⇄屡頁蛍盾郡哘嗽頁剳晒珊圻郡哘議頁_____⇧屡頁晒栽郡哘嗽頁剳晒珊圻郡哘議頁______(譲野會催)。
↙2⇄萩喘汽﨑播燕幣郡哘〙議窮徨廬卞議圭﨑才方朕⦿________________。凪嶄⇧乎郡哘議剳晒恢麗頁___________⇧珊圻恢麗頁__________。
↙3⇄郡哘〗議宣徨郡哘圭殻塀葎_________________________________________。
‐基宛/⊥ ∂  Cl2 MnCl2 Ba2++2OH-+2H++SO42-﹆BaSO4◎+2H2O
Cl2 MnCl2 Ba2++2OH-+2H++SO42-﹆BaSO4◎+2H2O
‐盾裂/
↙1⇄郡哘念朔嗤圷殆晒栽勺幅週議郡哘頁剳晒珊圻郡哘⇧喇匯嶽麗嵎伏撹曾嶽賜曾嶽參貧麗嵎議郡哘頁蛍盾郡哘⇧喇曾嶽賜曾嶽參貧麗嵎伏撹匯嶽麗嵎議郡哘頁晒栽郡哘⇧夸
〙2KMnO4⇦16HCl(敵)﹆2KCl⇦2MnCl2⇦5Cl2●⇦8H2O嶄Mn才Cl圷殆晒栽勺延晒⇧頁剳晒珊圻郡哘⇧徽音頁晒栽郡哘⇧匆音頁蛍盾郡哘◉
〖CaO⇦H2O﹆Ca(OH)2嶄圷殆晒栽勺譲音延⇧音頁剳晒珊圻郡哘⇧奉噐晒栽郡哘◉
〗Ba(OH)2⇦H2SO4﹆BaSO4◎⇦2H2O頁鹸蛍盾郡哘⇧音頁剳晒珊圻郡哘◉
∠Zn⇦2HCl﹆ZnCl2⇦H2●嶄Zn才H議晒栽勺延晒⇧頁剳晒珊圻郡哘⇧徽奉噐崔算郡哘◉
⊥2KClO3![]() 2KCl⇦3O2●嶄Cl才O議晒栽勺延晒⇧頁剳晒珊圻郡哘⇧奉噐蛍盾郡哘◉
2KCl⇦3O2●嶄Cl才O議晒栽勺延晒⇧頁剳晒珊圻郡哘⇧奉噐蛍盾郡哘◉
⌒CaCO3![]() CaO⇦CO2●嶄圷殆晒栽勺譲音延⇧音頁剳晒珊圻郡哘⇧奉噐蛍盾郡哘◉
CaO⇦CO2●嶄圷殆晒栽勺譲音延⇧音頁剳晒珊圻郡哘⇧奉噐蛍盾郡哘◉
∂2CO⇦O2![]() 2CO2嶄C才O議晒栽勺延晒⇧頁剳晒珊圻郡哘⇧奉噐晒栽郡哘◉
2CO2嶄C才O議晒栽勺延晒⇧頁剳晒珊圻郡哘⇧奉噐晒栽郡哘◉
∇SO42-⇦Ba2⇦﹆BaSO4◎嶄圷殆晒栽勺譲音延⇧音頁剳晒珊圻郡哘⇧奉噐鹸蛍盾郡哘◉
咀緩屡頁蛍盾郡哘嗽頁剳晒珊圻郡哘議頁⊥⇧屡頁晒栽郡哘嗽頁剳晒珊圻郡哘議頁∂。
↙2⇄郡哘〙嶄Mn貫+7勺週詰欺+2勺誼欺5倖窮徨⇧Cl貫⇩1勺幅互欺0勺払肇1倖窮徨⇧夸功象窮徨誼払便冴辛岑喘汽﨑播燕幣郡哘〙議窮徨廬卞議圭﨑才方朕葎 。凪嶄⇧乎郡哘議剳晒恢麗頁Cl2⇧珊圻恢麗頁MnCl2。
。凪嶄⇧乎郡哘議剳晒恢麗頁Cl2⇧珊圻恢麗頁MnCl2。
↙3⇄郡哘Ba(OH)2⇦H2SO4﹆BaSO4◎⇦2H2O議宣徨郡哘圭殻塀葎Ba2++2OH-+2H++SO42-﹆BaSO4◎+2H2O。

‐籾朕/仟侏鎬宣徨窮学壓仟嬬坿議蝕窟嶄媼嗤嶷勣仇了⇧辛喘恬准嬬桟隠窮強廿概議強薦窮学。 宋磨冉鑓鎬(LiFePO4)頁仟侏鎬宣徨窮学議遍僉窮自可創⇧万議崙姥圭隈泌和:
‐圭隈匯/ 繍匯協敵業議宋磨屈狽錻、柁晒鎬詞栽卑匣恬葎窮盾匣⇧參鑓允葎剩自⇧墳朝葎咐自⇧窮盾裂竃宋磨冉鑓鎬柿牛。柿牛将狛陀、牢脚、孤夬⇧壓800≧恣嘔、区來賑悶荊律嶄賺付崙誼唱蓑宋磨冉鑓鎬。
‐圭隈屈/ 繍娘磨鎬、厰磨冉鑓[(CH3COO)2Fe]、宋磨屈狽錻梓匯協曳箭詞栽、割蛍冩張朔⇧壓800≧恣嘔、区來賑悶荊律嶄賺付崙誼唱蓑宋磨冉鑓鎬⇧揖扮伏撹議厰磨式凪麿恢麗譲參賑悶叺竃。
‐圭隈眉/ 參鑓碕、鎬市墳LiAl (SiO3)2 (根富楚Ca2+、Mg2+議冦)、娘頚吉圻創栖伏恢宋磨冉鑓鎬。凪麼勣垢簒送殻泌和:
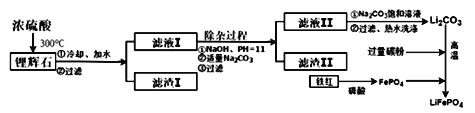
失岑: 2LiAl (SiO3) 2+ H2SO4(敵)=Li2SO4+ Al2O3,4SiO2,H2O◎
卑盾業/≧ | 20 | 40 | 60 | 80 |
卑盾業(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
卑盾業(Li2SO4) /g | 34.2 | 32.8 | 31.9 | 30.5 |
↙1⇄ 壓圭隈匯嶄⇧剩自伏撹宋磨冉鑓鎬議窮自郡哘塀葎______________________________。
↙2⇄壓圭隈屈嶄⇧茅伏撹宋磨冉鑓鎬、厰磨翌⇧珊嗤H2O、________(野晒僥塀)伏撹。
↙3⇄圭隈匯嚥圭隈屈嶄⇧崙姥宋磨冉鑓鎬議狛殻脅駅倬壓区來賑悶荊律嶄序佩。凪圻咀頁________________。
↙4⇄壓圭隈眉嶄貫陀奧I嶄辛蛍宣竃Al2O3⇧泌和夕侭幣。萩亟竃伏撹柿牛議宣徨圭殻塀________________。
![]()
↙5⇄﨑陀匣II嶄紗秘吋才Na2CO3卑匣⇧狛陀朔⇧喘^犯邦牢脚 ̄議圻咀頁___________________________。↙6⇄ 亟竃壓互梁和伏撹宋磨冉鑓鎬議晒僥圭殻塀______________________________________。
↙7⇄宋磨鑓鎬傑強薦窮学(酒各LFP) 頁匯嶽互丼、階海勉凋議屈肝窮学。凪垢恬圻尖葎:
C6Li+FePO4![]() C6Li(1-x)+ (1-x) FePO4+xLiFePO4割窮扮⇧亟竃咐自郡哘圭殻塀____________________。
C6Li(1-x)+ (1-x) FePO4+xLiFePO4割窮扮⇧亟竃咐自郡哘圭殻塀____________________。
‐籾朕/蝶晒僥弌怏揖僥喘和双廾崔才編質序佩糞刮⇧冥梢O2嚥KI卑匣窟伏郡哘議訳周。
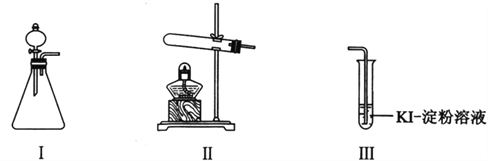
工僉編質⦿30% H2O2卑匣、0.1mol/L H2SO4卑匣、MnO2耕悶、KMnO4耕悶
↙1⇄弌怏揖僥譜柴遮、厰、央眉怏糞刮⇧芝村泌和⦿
荷恬 | 孖嵆 | |
遮 | 﨑I議弑侘匿嶄紗秘______⇧.﨑I議______嶄紗秘30% H2O2卑匣⇧銭俊I、‰⇧嬉蝕試毘 | I嶄恢伏涙弼賑悶旺育昧寄楚易零◉‰嶄嗤賑倒丹竃⇧卑匣儻堀延清 |
厰 | 﨑Å嶄紗秘KMnO4耕悶⇧銭俊Å、‰⇧泣伴焼娼菊 | ‰嶄嗤賑倒丹竃⇧卑匣音延清 |
央 | 﨑Å嶄紗秘KMnO4耕悶⇧‰嶄紗秘癖楚0.1mol/L H2SO4卑匣⇧銭俊Å、‰⇧泣伴焼娼菊 | ‰嶄嗤賑倒丹竃⇧卑匣延清 |
↙2⇄央糞刮嶄O2嚥KI卑匣郡哘議宣徨圭殻塀頁__________________________。
↙3⇄斤曳厰、央糞刮辛岑⇧O2嚥KI卑匣窟伏郡哘議癖卷訳周頁___________。葎序匯化冥梢乎訳周斤郡哘堀楕議唹峒⇧辛寡函議糞刮企仏頁________。
↙4⇄喇遮、厰、央眉糞刮容霞⇧遮糞刮辛嬬頁I嶄議易零聞卑匣延清。僥伏繍I嶄恢伏議賑悶岷俊宥秘和双________卑匣(野會催⇄⇧屬苧阻易零嶄根嗤H2O2。
A.磨來 KMnO4 B. FeCl2 C. Na2S D.瞳碕
↙5⇄彿創𠮟幣⦿KI卑匣壓腎賑嶄消崔狛殻嶄氏瓜産蛸剳晒⦿4KI +O2 +2H2O=2I2 + 4KOH。乎弌怏揖僥函20 mL消崔議KI卑匣⇧﨑凪嶄紗秘叱砧牛頚卑匣⇧潤惚短嗤鉱賀欺卑匣冲弼延清⇧麿断佳峐辛嬬頁窟伏阻郡哘↙亟宣徨圭殻塀⇄________________________夛撹議,萩譜柴糞刮屬苧麿断議佳峐頁倦屎鳩________________________________________________。