题目内容
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是 ( )
A. 在NaClO和NaCl的混合溶液中,Ag+、K+、NO3-、I-可以大量共存
B. Kw/C(H+) =1×10-13mol·L-1的溶液中: NH4+、Ca2+、Cl-、NO3-
C. ![]() 在溶液中能大量共存,通过量
在溶液中能大量共存,通过量![]() 后仍能大量共存
后仍能大量共存
D. 水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、Al![]() 、C
、C![]()
【答案】B
【解析】A. 在NaClO和NaCl的混合溶液中Ag+转化氯化银沉淀,I-被次氯酸钠氧化,均不能大量共存,A错误;B. Kw/c(H+) =1×10-13mol·L-1的溶液中氢离子浓度大于氢氧根浓度,溶液显酸性,NH4+、Ca2+、Cl-、NO3-之间不反应,可以大量共存,B正确;C. 通过量CO2后硅酸根转化为硅酸沉淀,不能大量共存,C错误;D. 水电离的c(H+)=1×10-13mol·L-1的溶液中水的电离被抑制,如果溶液显酸性,则偏铝酸根离子和碳酸根离子均不能大量共存,D错误,答案选B。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案【题目】以硼镁泥(主要成分为MgSiO3、Fe2O3及少量Al2O3、FeO和MnO)为原料制备高纯Mg(OH)2的流程如下:
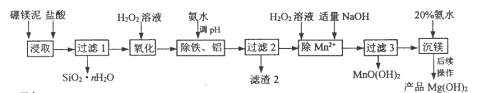
己知:
①常温下此体系中各氢氧化物开始沉淀与沉淀完全时的pH范围如下表所示:
pH值 | Mg(OH)2 | Mn(OH)2 | MnO(OH)2 | Fe(OH)2 | Al(OH)3 | Fe(OH)3 |
开始沉淀时 | 9.3 | 7.1 | 7.8 | 7.6 | 3.7 | 2.3 |
沉淀完全时 | 10.8 | 10.8 | 9.8 | 9.6 | 4.7 | 3.7 |
②温度高于340℃时Mg(OH)2开始分解为MgO和H2O。
(1)“浸取”时,为提高镁的浸取率可行的措施为__________。
a.将硼镁泥制成浆料 b.降低浸取温度 c.用盐酸多次浸取
(2)“浸取”时,MgSiO3与盐酸反应的化学方程式为_________________________。
(3)“除铁、铝”时,需调节溶液pH范围为_________________________。
(4)“除Mn2+”时发生反应的离子方程式为_________________________;
过滤3所得滤渣中含有MnO(OH)2和__________。
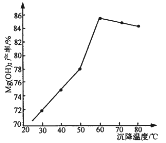
(5)“沉镁”时,反应温度与Mg(OH)2的产率如图所示,当温度超过60℃,随温度再升高,Mg(OH)2产率反而降低,其原因可能是________________。