题目内容
【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为CO(g)+2H2(g)=CH3OH(g) ΔH=-116kJ·mol-1。某些化学键的键能数据如表:
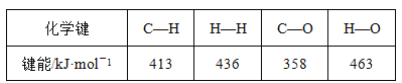
则CO中碳氧键的键能是
A.431kJ·mol-1B.946kJ·mol-1
C.1072kJ·mol-1D.1130kJ·mol-1
【答案】C
【解析】
CO(g)+2H2(g)CH3OH (g)的焓变=反应物总键能之和-生成物总键能之和,设CO中碳氧键的键能为x,结合图表提供的化学键的键能,则△H═x+2×436kJ/mol-(3×413kJ/mol+358kJ/mol+463kJ/mol)=-116 kJmol-1,解得:x=1072kJ/mol,故答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目