题目内容
化学工业上生产尿素的化学反应是:CO2+2NH3==CO(NH2)2+H2O。已知下列物质在一定条件下均能与水反应产H2和CO2,H2是合成氨的原料,CO2供合成尿素用。若从原料被充分利用的角度考虑,选用_____作原料较好。
| A.CO | B.石脑油(C5H12、C6H14) | C.CH4 | D.焦炭 |
B
根据反应 N2+3H2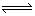 2NH3;CO2+2NH3=CO(NH2)2+H2O,若要充分利用原料,显然在原料与水反应产生的H2和CO2物质的量之比等于或接近于3:1时,上述反应趋于恰好完全反应,原料得以充分利用。根据提示信息:
2NH3;CO2+2NH3=CO(NH2)2+H2O,若要充分利用原料,显然在原料与水反应产生的H2和CO2物质的量之比等于或接近于3:1时,上述反应趋于恰好完全反应,原料得以充分利用。根据提示信息:
C+2H2O=CO2+2H2(2:1);
CO+H2O=CO2+H2(1:1);
CH4+2H2O=4H2(4:1);
C5H12+10H2O=5CO2+16H2(3.2:1),
C6H14+12H2O=6CO2+19H2(3.17:1),
故石油脑的利用率最高。
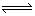 2NH3;CO2+2NH3=CO(NH2)2+H2O,若要充分利用原料,显然在原料与水反应产生的H2和CO2物质的量之比等于或接近于3:1时,上述反应趋于恰好完全反应,原料得以充分利用。根据提示信息:
2NH3;CO2+2NH3=CO(NH2)2+H2O,若要充分利用原料,显然在原料与水反应产生的H2和CO2物质的量之比等于或接近于3:1时,上述反应趋于恰好完全反应,原料得以充分利用。根据提示信息: C+2H2O=CO2+2H2(2:1);
CO+H2O=CO2+H2(1:1);
CH4+2H2O=4H2(4:1);
C5H12+10H2O=5CO2+16H2(3.2:1),
C6H14+12H2O=6CO2+19H2(3.17:1),
故石油脑的利用率最高。

练习册系列答案
相关题目

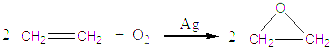
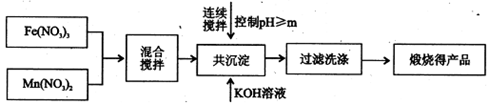
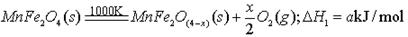
 (填字母编号)。
(填字母编号)。 B.物料可循环使用
B.物料可循环使用