题目内容
下列有关金属的冶炼说法不正确的是
| A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化 |
| B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应 |
| C.用磁铁矿炼失的反应中,1molFe3O4被CO还原成Fe时,转移9mole- |
| D.铝热法还原铁的反应中,放出的热量能使铁熔化 |
C
略

练习册系列答案
相关题目
 2NH3(g),其
2NH3(g),其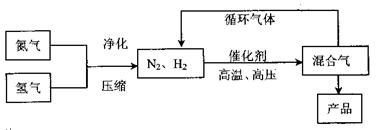
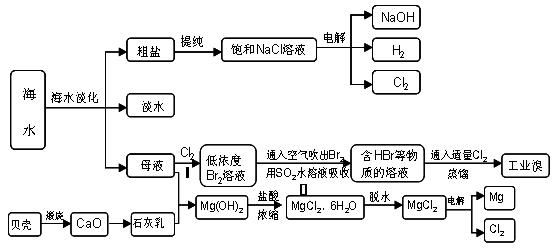

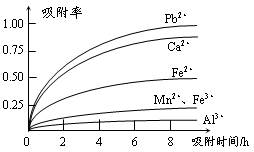
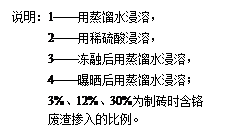
 Cr(OH)3
Cr(OH)3 CrO2-① FeSO4还原Cr2O72-的离子方程式为 。
CrO2-① FeSO4还原Cr2O72-的离子方程式为 。