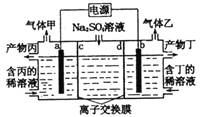
题目内容
【题目】下列各组离子能大量共存的是( )
A.Mg2+、H+、Cl-、HCO3-B.K+、NH4+、NO3-、CO32-
C.NH4+、Na+、SO42-、OH-D.Ag+、Cu2+、Cl-、SO42-
【答案】B
【解析】
A.H+和HCO3-会发生反应生成二氧化碳和水,不能大量共存,故A错误;
B.K+、NH4+、NO3-、CO32-离子之间不发生任何化学反应,可大量共存,故B正确;
C.NH4+和OH-结合生成一水合氨,不能大量共存,故C错误;
D.Ag+和Cl-结合生成氯化银沉淀,不能大量共存,故D错误;
答案选B。

【题目】已知:相关物质的溶度积常数见表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10﹣20 | 2.6×10﹣39 | 1.7×10﹣7 | 1.3×10﹣12 |
现有某酸性CuCl2溶液中含有少量的FeCl2 , 为得到纯净的CuCl22H2O晶体,按如图步骤进行提纯:
(1)最适合作氧化剂X的是(填字母),加入X的目的是 . A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
加入的物质Y是(填化学式),调至溶液pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= . 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体.
(2)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I﹣发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000molL﹣1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.(I2+2S2O32﹣═S4O62﹣+2I﹣)①可选用作滴定指示剂.②CuCl2溶液与KI反应的离子方程式为 .
③该试样中CuCl22H2O的质量百分数为 .