题目内容
将19.0g甲烷和乙烯的混合气体通入足量的溴水后,溴水增重7.0g,则混合气体中甲烷的体积分数是( )
| A、25% | B、50% |
| C、63.2% | D、75% |
考点:化学方程式的有关计算
专题:有机物的化学性质及推断
分析:甲烷不与溴水反应,乙烯能与溴水反应生成二溴乙烷,说明乙烯的质量为7.0g,根据n=
计算乙烯的物质的量,再根据m=nM进而计算乙烯的质量,然后求混合气体中甲烷的体积分数.
| m |
| M |
解答:
解:甲烷不与溴水反应,乙烯能与溴水反应生成二溴乙烷,说明乙烯的质量为7.0g,故乙烯的物质的量=
=0.25mol,所以乙烯的质量为0.25mol×28g/mol=7g,故甲烷的物质的量=
mol=0.75mol,则混合气体中甲烷的体积分数
×100%=75%,
故选D.
| 7.0g |
| 28g/mol |
| 19-7 |
| 16 |
| 0.75mol |
| 0.75mol+0.25mol |
故选D.
点评:本题考查混合物的计算,难度不大,注意乙烯与甲烷的性质的差异性,确定溴水增重为乙烯的质量是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是( )
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1 ②2H2(l)+O2(l)═2H2O(g)△H=-482.6kJ?mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷 (C3H8) |
③C3H8(l)+5O2(g)═3CO2(g)+4H2O(g)△H=-2013.8kJ?mol-1 ④C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2221.5kJ?mol-1 |
| A、571.6 kJ?mol-1,2 221.5 kJ?mol-1 |
| B、241.3 kJ?mol-1,2 013.8 kJ?mol-1 |
| C、285.8 kJ?mol-1,2 013.8 kJ?mol-1 |
| D、285.8 kJ?mol-1,2 221.5 kJ?mol-1 |
目前冰箱中使用的致冷剂是氟里昂(CF2Cl2),下面关于该氟里昂的说法正确的是( )
| A、没有固定的熔沸点 |
| B、分子中的碳原子是饱和的碳原子 |
| C、属于正四面体的空间结构 |
| D、可能有两种结构 |
化学充实了生活、改变了生活,下列相关说法正确的是( )
| A、NaHCO3能与碱反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
| B、石油的催化裂解是为了提高从石油中得到汽油等轻质油的产量 |
| C、常用的消毒剂氯气和调料乙酸,两者都含有非极性共价键 |
| D、废旧电池有牢固外壳保护不会污染土壤和水体,故不必回收处理 |
常温下,下列各组粒子在指定溶液中可能大量共存的是( )
| A、氨水中:Al3+、Cl-、I-、SO42- |
| B、pH=2的溶液中:K+、Cu2+、Cl-、NO3- |
| C、食盐水中:Mg2+、Fe(OH)2、Br-、CO32- |
| D、无色溶液:NO3-、SO2、NH4+、Na+ |
下列化学用语表达错误的是( )
A、原子核内有18个中子的氯原子:
| ||
B、NH4Br的电子式: | ||
C、Mg的原子结构示意图为: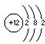 | ||
| D、丙烯的结构简式:CH3CH=CH2 |
下列物质可用铁桶盛装的是( )
| A、浓HCl |
| B、CuSO4 |
| C、0.5mol/L HNO3 |
| D、ρ=1.84g/cm3,98%H2SO4 |