题目内容
【题目】Ⅰ.在![]() C、
C、![]() N、
N、![]() O、
O、![]() Cl、
Cl、![]() U、
U、![]() U中:
U中:
(1)___和_____的质量数相等,但不能互称为同位素。
(2)____和__的中子数相等,但质子数不相等,所以不是同一种元素。以上所列共有____种元素。
Ⅱ.物质的类别和核心元素的化合价是研究物质性质的两个基本视角。

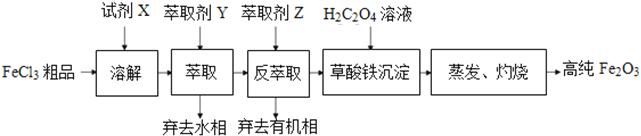
(1)Y的分子式为____。
(2)图中X的电子式为 H![]() H ;其水溶液长期在空气中放置容易变浑浊,原因是____(用化学方程式表示);该变化体现出:S非金属性比O____(填“强”或“弱”)。用原子结构解释原因:同主族元素从上到下,__________,得电子能力逐渐减弱。
H ;其水溶液长期在空气中放置容易变浑浊,原因是____(用化学方程式表示);该变化体现出:S非金属性比O____(填“强”或“弱”)。用原子结构解释原因:同主族元素从上到下,__________,得电子能力逐渐减弱。
(3)Z与图表中某物质反应生成SO2的化学方程式是_______。
【答案】 ![]() C
C ![]() N
N ![]() C
C ![]() O 5 SO3_ 2H2S+O2===2S↓+2H2O 弱 电子层数增多,原子半径增大 Na2SO3+H2SO4===Na2SO4+SO2↑+H2O
O 5 SO3_ 2H2S+O2===2S↓+2H2O 弱 电子层数增多,原子半径增大 Na2SO3+H2SO4===Na2SO4+SO2↑+H2O
【解析】本题主要考查硫酸、亚硫酸钠等物质的性质。
Ⅰ.(1) ![]() C和
C和![]() N的质量数相等,但不能互称为同位素。
N的质量数相等,但不能互称为同位素。
(2) ![]() C 和
C 和![]() O的中子数相等,但质子数不相等,所以不是同一种元素。
O的中子数相等,但质子数不相等,所以不是同一种元素。
以上所列共有C、N、O、Cl、U5种元素。
Ⅱ.(1)Y的分子式为SO3。
(2)图中X是硫化氢,其电子式为 H![]() H;其水溶液长期在空气中放置容易变浑浊,原因是2H2S+O2===2S↓+2H2O;该变化体现出:S非金属性比O弱。用原子结构解释原因:同主族元素从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱。
H;其水溶液长期在空气中放置容易变浑浊,原因是2H2S+O2===2S↓+2H2O;该变化体现出:S非金属性比O弱。用原子结构解释原因:同主族元素从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱。
(3)Z是亚硫酸钠,亚硫酸钠与硫酸反应生成SO2,该反应的化学方程式是Na2SO3+H2SO4===Na2SO4+SO2↑+H2O。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目