题目内容
【题目】![]() 为周期表中前20号元素中的四种,原子序数依次增大,
为周期表中前20号元素中的四种,原子序数依次增大,![]() 为金属元素,
为金属元素,![]() 原子的最外层电子数是次外层电子数的3倍,
原子的最外层电子数是次外层电子数的3倍,![]() 位于同周期,
位于同周期,![]() 单质是一种良好的半导体.
单质是一种良好的半导体.![]() 能与冷水剧烈反应,
能与冷水剧烈反应,![]() 原子的最外层电子数之和与
原子的最外层电子数之和与![]() 原子的最外层电子数之和相等.下列说法正确的是
原子的最外层电子数之和相等.下列说法正确的是
A. 原子半径:![]() B. 气态氢化物的稳定性:
B. 气态氢化物的稳定性:![]()
C. 最高价氧化物对应水化物的碱性:![]() D.
D. ![]()
![]() 中共价键的数目为
中共价键的数目为![]()
【答案】A
【解析】
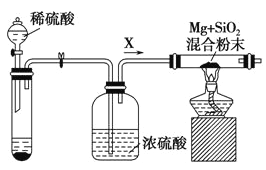
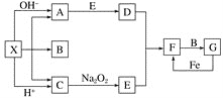
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,X原子的最外层电子数是次外层电子数的3倍,则X有2个电子层,最外层电子数为6,故X为氧元素;Z单质是一种良好的半导体,Z为硅元素。W、Y为金属元素,且w原子序数大于还能和冷水反应,所以w为K,Y、Z位于同周期,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,故Y为铝元素,即X为氧元素,Y为铝元素,Z为硅元素,W为钾元素。
A.同周期随原子序数增大,原子半径减小,同主族自上而下,原子半径增大,所以原子半径,K![]() Al
Al ![]() Si
Si ![]() O即W>Y>Z>X,故A正确;
O即W>Y>Z>X,故A正确;
B.X为氧元素,Z为硅元素,同主族自上而下非金属性减弱,所以非金属性![]() ,非金属性越强,氢化物越稳定,所以气态氢化物稳定性X>Y,故B错误;.
,非金属性越强,氢化物越稳定,所以气态氢化物稳定性X>Y,故B错误;.
C.Y为铝元素,W为钾元素,同主族自上而下金属性增强,所以金属性![]() ,同周期自左而右金属性减弱,所以金属性
,同周期自左而右金属性减弱,所以金属性![]() ,金属性
,金属性![]() ,金属性越强,最高价氧化物对应水化物的碱性越强,所以碱性Y<W,故C错误;
,金属性越强,最高价氧化物对应水化物的碱性越强,所以碱性Y<W,故C错误;
D.SiO2是原子晶体,1个O原子周围有2个Si原子,1个Si原子周围有4个O原子,![]()
![]() 中共价键的数目为
中共价键的数目为![]() ,故D错误;
,故D错误;
本题答案为A。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目