题目内容
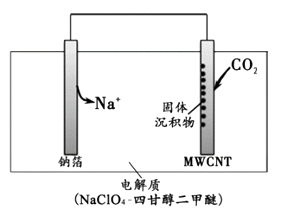
【题目】工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3:PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
A.PbSO4的溶解度小于PbCO3
B.处理PbSO4后,Na2CO3或NaHCO3溶液的pH升高
C.若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4 , Na2CO3溶液中的PbSO4转化率较大
D.整个过程涉及一个复分解反应和两个氧化还原反应
【答案】C
【解析】A.根据方程式,PbCO3的溶解度小于PbSO4,故A不符合题意;
B. 处理PbSO4后,Na2CO3或NaHCO3溶液转变为硫酸钠溶液,pH降低,故B不符合题意;
C. 若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4,碳酸氢钠的电离程度较小,碳酸根离子浓度较小,而碳酸钠中碳酸根离子浓度较大,Na2CO3溶液中的PbSO4转化率较大,故C符合题意;
D. 整个过程涉及两个复分解反应:PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42—(aq)和PbCO3灼烧后获得PbO,一个氧化还原反应:PbO转变为Pb,故D不符合题意。
PbCO3(s) + SO42—(aq)和PbCO3灼烧后获得PbO,一个氧化还原反应:PbO转变为Pb,故D不符合题意。
所以答案是:C

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案【题目】探究并回答问题
(1)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| A | B | C | D | E | F |
4molL﹣1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1= , V6= , V9=;
②反应一段时间后,实验A中的金属呈色,实验E中的金属呈色;
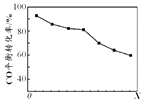
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高.但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因 .
(2)在100℃和200kPa的条件下,反应aA(g)bB(g)+cC(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维持温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度.
压强(kPa) | 200 | 500 | 1 000 |
B的浓度(molL﹣1) | 0.04 | 0.1 | 0.27 |
根据表中的数据,回答下列问题:
①压强从200kPa增加到500kPa时,平衡移动(填“正向”“逆向”或“不”),理由是 .
②压强从500kPa增加到1 000kPa时,平衡转移(填“正向”“逆向”或“不”),其原因可能是 .