题目内容
【题目】将3 molO2加入到V L的反应器中,在高温下放电,经t1 s建立了平衡体系:3O2![]() 2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
A. 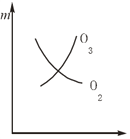 B.
B. 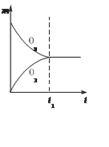
C. 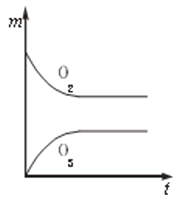 D.
D. 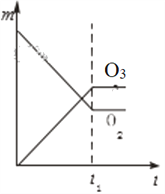
【答案】C
【解析】试题O2的转化率为30%,则O2的消耗量为3mol×30%=0.9mol,则
3O2![]() 2O3
2O3
n(始):3 0
n(变):0.9 0.6
n(平):2.1 0.6
O2的起始浓度为3mol/VL,O2的平衡浓度为2.1mol/VL,O3的起始浓度为0,O3的平衡浓度为0.6mol/VL,A、图像表示平衡时O2和O3的物质的量相同,与实际不符,A错误;B、图像表示平衡时O2和O3的物质的量相同,与实际不符,B错误;C、图像表示平衡时O2的物质的量大于O3的物质的量,与实际相符,C正确;D、图像表示平衡时O2的物质的量小于O3的物质的量,与实际不符,D错误,答案选C。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
【题目】下表是一些烷烃的燃烧热,则下列表达正确的是
化合物 | 燃烧热/ kJ·mol-1 | 化合物 | 燃烧热/ kJ·mol-1 |
甲烷 | 891.0 | 正丁烷 | 2878.0 |
乙烷 | 1560.8 | 异丁烷 | 2869.6 |
丙烷 | 2221.5 | 异戊烷 | 3531.3 |
A. 正戊烷的燃烧热大于3531.3 kJ·mol-1
B. 相同质量的烷烃、碳的质量分数越大,燃烧放出的热量越多
C. 正丁烷转化为异丁烷的热化学方程式为:CH3CH2CH2CH3(g) ![]() CH3CH(CH3)CH3(g) △H =+8.4kJ·mol-1
CH3CH(CH3)CH3(g) △H =+8.4kJ·mol-1
D. 甲烷燃烧的热化学方程式为:CH4(g)+2O2(g) ![]() CO2(g) +2H2O(g) △H =-891.0kJ·mol-1
CO2(g) +2H2O(g) △H =-891.0kJ·mol-1