题目内容
下列各溶液中NO3-物质的量浓度最大的是
| A.20 mL 2 moL/L Mg(NO3)2 | B.100 mL 2.5 mot/L NaNO3 |
| C.25 mL 1.0mol/L Al(NO3)3 | D.30 mL 2.5 mol/L NH4NO3 |
A
解析试题分析:电解质产生的离子的浓度等于电解质的浓度与化学式中该离子的个数的乘积。A C(NO3-)="2×2" moL/L="4" moL/L。B C(NO3-)="1×1.5" moL/L="1.5" moL/L。C C(NO3-)=3×1.0moL/L="3" moL/L。D C(NO3-)="1×2" .5moL/L="2.5" moL/L。所以浓度最大的是A。
考点:考查电解质的浓度与电解质产生的离子的浓度的关系的知识。

练习册系列答案
相关题目
下列说法正确的是:①Cl-的结构示意图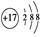 ;②羟基的电子式:·····H;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32—;⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化
;②羟基的电子式:·····H;③HClO的结构式:H—Cl—O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32—;⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化
| A.①②⑤ | B.①④⑥⑦ | C.②③④⑥ | D.②③⑤⑥⑦ |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B.18g水含有电子数为8NA |
| C.1L 0.3mol·L-1Na2SO4溶液中,含有Na+和SO42- 总数为0.6NA |
| D.NA个氢气分子(H2)的质量为2g |
设NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.1 mol苯分子中含有C=C双键数为3NA |
| B.1 mol甲基(—CH3)所含的电子总数为10 NA |
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为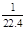 NA NA |
| D.4.2 g乙烯和丙烯的混合气体中所含碳原子数为0.3NA |
下列说法中正确的是( )
| A.一定条件下下向1L容器内通入46gNO2 ,则NO2 的物质的量浓度一定为1mol/L |
| B.标准状况下,22.4L的己烷中有20 x 6.02 x 1023个原子 |
| C.1mol氯气溶于水转移 6.02 x 1023个e- |
| D.0.1mol CH5+含6.02×1023个电子 |
NA表示阿伏加德罗常数的值,下列说法正确的是
| A.7.8 g Na2O2中含有的离子总数目为0.4NA |
| B.1mol 苯分子中含有碳碳双键数目为3NA |
| C.标准状况下,将分子总数为NA的NH3和HCl气体混合后的体积约为22. 4L |
| D.16g CH4与18 g NH4+所含电子数均为10NA |
设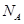 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,4g CH4含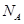 个共价键 个共价键 |
B.常温常压下,22.4L氦气含有的原子数为2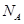 |
C.1molS在足量O2中燃烧,转移的电子数为6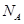 |
D.0.1 mol/L的碳酸氢钠溶液中含钠离子数为0.1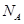 。 。 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温下,23g NO2含有NA个氧原子 |
| B.1 L 0.1 mol·L-1的氨水含有0.1NA个OH- |
| C.标准状况下,22.4 L CCl4含有NA 个CCl4分子 |
| D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A.12.5mL 16mol·L-1浓硫酸与足量锌反应,转移电子数为0.2NA |
| B.0.1 mol24Mg18O晶体中所含中子总数为2.0 NA |
| C.1L 1 mol·L-1的醋酸溶液中离子总数为2NA |
| D.4.5 g SiO2晶体中含有的硅氧键数目为0.3 NA |