题目内容
【题目】下列实验装置错误的是( )
A.乙炔的制取和收集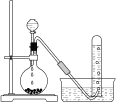 B.苯的硝化反应
B.苯的硝化反应
C.乙酸乙酯的制取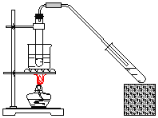 D.乙烯的制取
D.乙烯的制取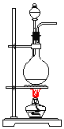
【答案】D
【解析】
A乙炔由碳化钙和水反应生成乙炔,选择固液不加热制取装置,乙炔微溶于水,可以用排水法收集, 故A正确;
B.苯的硝化反应,苯与浓硫酸在催化剂作用下可生成硝基苯,实验温度需控制在50-60℃ 长玻璃管可以起到冷凝回流的作用,故B正确;
C.乙酸与乙醇在浓硫酸作用下发生取代反应生成乙酸乙酯,温度应控制在60-70℃ 如温度太高会产生乙醚和亚硫酸等杂质,减少乙酸乙酯的产率,故可以选择水浴加热,故C正确;
D. 乙烯的制取且需要测定反应液的温度为170℃,需要温度计插入乙醇和浓硫酸的混合液中,若温度控制不当,会产生乙醚等杂质,故D错误;
答案选D。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】某实验小组用100mL0.50mol/LNaOH溶液与60mL0.50mol/L硫酸进行中和热的测定。装置如图所示,回答下列问题:
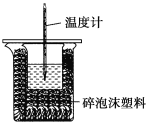
(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____g。
(2)图中装置缺少的仪器是____。
(3)硫酸稍过量的原因是____。
(4)请填写下表中的平均温度差:
实验 次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 平均温度差 (T2-T1)/℃ | ||
HCl | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ____ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(5)近似认为0.50 mol/L NaOH溶液与0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容为c=4.18J/(g℃)则上述实验中和热ΔH=___(取小数点后一位)
(6)上述实验结果与57.3kJ/mol有偏差产生偏差的原因可能是____
A.量取NaOH溶液时仰视读数
B.为了使反应充分,可以向酸中分次加入碱
C.实验装置保温隔热效果差
D.用铜丝代替玻璃棒搅拌