题目内容
A、B是两种同主族元素的原子,当它们都获得2个电子形成稳定结构的阴离子时,A放出的能量大于B,由此可知( )
分析:A与B两种元素的原子,当它们分别获得2个电子形成稳定结构的阴离子,说明最外层都有6个电子,位于周期表第ⅥA族,A放出的能量大于B,说明A的非金属性大于B,则原子序数A小于B,结合同主族元素性质的递变规律解答该题.
解答:解:A与B两种元素的原子,当它们分别获得2个电子形成稳定结构的阴离子,说明最外层都有6个电子,位于周期表第ⅥA族,A放出的能量大于B,说明A的非金属性大于B,则原子序数A小于B,则
A.A的非金属性大于B,则A的氢化物的稳定性大于B,故A正确;
B.素的非金属性越强,对应阴离子的还原性越弱,则B-还原性大于A-,故B错误;
C.原子序数A小于B,二者在同一主族,则A的原子半径小于B,故C错误;
D.同主族元素A、B获得2个电子形成稳定结构的阴离子时,A放出的能量大于B,说明A的非金属性大于B,故D错误.
故选A.
A.A的非金属性大于B,则A的氢化物的稳定性大于B,故A正确;
B.素的非金属性越强,对应阴离子的还原性越弱,则B-还原性大于A-,故B错误;
C.原子序数A小于B,二者在同一主族,则A的原子半径小于B,故C错误;
D.同主族元素A、B获得2个电子形成稳定结构的阴离子时,A放出的能量大于B,说明A的非金属性大于B,故D错误.
故选A.
点评:本题考查原子的结构与元素的性质,题目难度中等,注意从能量的角度判断元素的性质为解答该题的关键.

练习册系列答案
相关题目
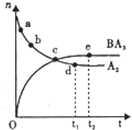 A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:
A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白: