题目内容
11.钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8,其中只有W显负价.X、Y的最外层电子数之和与Z的最高正价数相等,Y3+与W的阴离子具有相同的电子层结构,X、W的质子数之和等于Y、Z的质子数之和.下列说法错误的是( )| A. | 离子半径:X>Y | |
| B. | 氢化物的稳定性:W>Z | |
| C. | 化合物X2W2和Y2W3中都不含共价键 | |
| D. | 1 mol ZW2晶体所含Z-W键的数目为4NA(NA为阿伏加德罗常数的值) |
分析 只有W显负价,应为O元素,Y3+与W的阴离子具有相同的电子层结构,Y为Al元素,X、Y的最外层电子数之和与Z的最高正价数相等,可知该硅酸盐中,Z应为Si元素,X的化合价为+1价,X、W的质子数之和等于Y、Z的质子数之和,则X为K元素,该硅酸盐为KAlSi3O8,以此解答该题.
解答 解:只有W显负价,应为O元素,Y3+与W的阴离子具有相同的电子层结构,Y为Al元素,X、Y的最外层电子数之和与Z的最高正价数相等,可知该硅酸盐中,Z应为Si元素,X的化合价为+1价,X、W的质子数之和等于Y、Z的质子数之和,则X为K元素,该硅酸盐为KAlSi3O8.
A.K+比Al3+多一个电子层,K+离子半径较大,故A正确;
B.非金属性O>Si,元素的非金属性越强,对应的氢化物越稳定,故B正确;
C.K2O2、Al2O3两种化合物都为离子化合物,K2O2含有离子键和共价键,而Al2O3只含有离子键,故C错误;
D.在二氧化硅中,每个硅原子周围有4个Si-O键,所以lmolSiO2晶体所含Si-O键的数目为4NA,故D正确
故选C.
点评 本题考查原子结构与元素周期律,推断元素是解答关键,D选项为易错点,中注意熟记中学常见的晶体结构.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
2. 科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )
 科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )| A. | 羟基硝酸铵中阳离子的各原子共平面 | |
| B. | 羟基硝酸铵是离子化合物 | |
| C. | 羟基硝酸铵中含有离子键和共价键 | |
| D. | 9.6g羟基硝酸铵中含有0.2mol离子 |
19.NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,11.2L NO和O2混合气体的原子数为NA | |
| B. | 15g甲基所含有的电子数目为9NA | |
| C. | 1L0.1mol/L的氨水溶液中含有的N原子数大于0.1NA | |
| D. | 标准状况下,6.72L NO2与水反应转移电子数为0.4NA |
16.下列说法正确的是( )
| A. | 铝和铜常用于导电体,铝被人类大规模开发、使用的时间远超过铜被人类大规模开发和使用的时间 | |
| B. | 使用煤液化的产品作燃料与直接燃烧煤比较,对保护环境有利,目前,煤液化的唯一途径是将煤在高温和催化剂条件下与氢气反应 | |
| C. | 石油分馏的馏分之一是石油气,石油气含有大量的己烷 | |
| D. | 在陶瓷、聚合物中加入固态胶体粒子,可以改进材料的耐冲击强度和耐断裂强度 |
3.乙酸橙花酯是一种食用香料,其结构简式如图所示.下列关于该有机物的叙述中不正确的是( )

| A. | 分子式为C12H20O2 | |
| B. | 能发生加成反应、取代反应、氧化反应 | |
| C. | 1mol该有机物在一定条件下能和3mol H2发生反应 | |
| D. | 该有机物仅含有两种不同类型的官能团 |
1.短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与其他三种元素原子的内层电子数相同.X、Y均能与Z分别形成原子个数比为1:1、1:2的气态化合物.根据以上叙述,下列说法不正确的是( )
| A. | 上述气态化合物分子中所有原子最外层电子数均为8 | |
| B. | X、Y、Z都可与W形成既有极性共价键又有非极性共价键的化合物 | |
| C. | 化合物W4XY2Z可能是离子化合物,也可能是共价化合物 | |
| D. | 沸点:W2Z>YW3>XW4 |

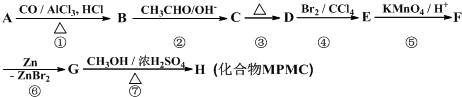

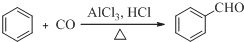
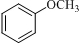 ;D
;D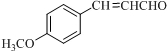 .
. .
.