��Ŀ����
����Ŀ����4.48LCO2ͨ��һ�����Ĺ���������ƺ��ռ���3.36L����(����IJ������ڱ�״����)�������������������
A. 3.2g B. 4.8g C. 5.4g D. 6g
���𰸡�D
����������μӷ�Ӧ��CO2��������Ϊa�����ɵ�O2�����Ϊb����
2CO2��2Na2O2=2Na2CO3��O2���������������V
2 1 1
a b 4.48L-3.36L=1.12L
��ã�a=2.24L��b=1.12L��
�������������1.12L��С��3.36L���ʶ�����̼��ʣ�࣬
���ԣ�3.36L������CO2���Ϊ4.48L-2.24L=2.24L��O2�����Ϊ1.12L��
����4.48L���������Ϊ![]() ��44g/mol+
��44g/mol+![]() ��32g/mol=6.0g����ѡD��
��32g/mol=6.0g����ѡD��
�㾦�����⿼����ݷ���ʽ�ļ��㣬�Ѷ��еȣ������ȡ���������㣬���Ա��ⵥ�����ۻ�����ж�����������ɣ�ע����������������������������������ͨ������������μӷ�Ӧ�Ķ�����̼��������ɵ�������������ж�3.36L�������ɼ����ɷֵ�������ٸ���n=![]() ����������������ʵ���������m=nM����������
����������������ʵ���������m=nM����������
�����͡���ѡ��
��������
26
����Ŀ��ij�����A������Al2(SO4)3��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ�ı仯����ش��������⡣
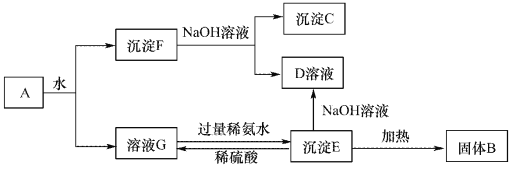
��1������F��NaOH��Һ��Ӧ�����˷���ʽΪ_______________��
��2������C��ϡ���ᷴӦ�����ӷ���ʽΪ_______________��
��3����ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����ʽΪ_______________��
���𰸡� Al2O3 + 2 OH��=AlO2��+H2O Fe2O3 + 6H�� =2 Fe3��+3H2O Al2��SO4��3 + 6NH3��H2O = 2Al��OH��3�� + 3��NH4��2SO4
���������������̿�֪��A����ˮ�ó�������Һ����ҺG����������Һ������F������������������
������F���ڹ���NaOH��Һ�У�Al2O3�ܺ��������Ʒ�Ӧ��Fe2O3���������Ʋ���Ӧ�����Գ���C��Fe2O3����ҺD��NaAlO2����ҺG�м�������İ�ˮ�õ�����E����EΪAl��OH��3��Al��OH��3��NaOH��Һ��Ӧ�õ�NaAlO2����Al��OH��3���ȵõ�����B��B��Al2O3���������Ͱ�ˮ��Ӧ����Al��OH��3������泥���1������F��NaOH��Һ��Ӧ�����ӷ���ʽΪ��Al2O3 + 2 OH��=AlO2��+H2O����2������CΪFe2O3��Fe2O3��ϡ���ᷴӦ�����ӷ���ʽΪ��Fe2O3 + 6H�� =2 Fe3��+3H2O����3����ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����ʽΪ��Al2(SO4)3 + 6NH3��H2O = 2Al(OH)3�� + 3(NH4)2SO4��