题目内容
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。
X | Y | ||||
Z | W | Q | |||
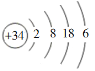
(1)Q的原子结构示意图是________。
(2)Y、Z、W形成简单离子,其离子半径关系为________(用离子符号表示)。
(3)用有关离子方程式表示Q、W元素的非金属性强弱______________
(4)Y的氢化物分子中含有18个电子,该分子中的共价键类型_____________________________。
(5)W的最高价氧化物对应的水化物的浓溶液与Cu反应的化学方程式为________________________。
【答案】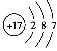 S2->O2->Al3+ S2-+Cl2===2Cl-+S↓ 极性共价键、非极性共价键 Cu+2H2SO4(浓)
S2->O2->Al3+ S2-+Cl2===2Cl-+S↓ 极性共价键、非极性共价键 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
【解析】
由图可知X、Y、Z、W、Q分别是N、O、Al、S、Cl,依据这些元素单质和化合物性质可解。
(1) Cl的原子结构示意图是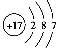 ;
;
(2) O、Al、S形成简单离子,S2-有三层电子,O2-和Al3+均有两层电子,但是O的核电荷数小,所以其离子半径关系为S2->O2->Al3+;
(3)氧化性氯气大于硫,表示S、Cl元素的非金属性强弱有关离子方程式:S2-+Cl2===2Cl-+S↓;
(4) O的氢化物分子中含有18个电子为H2O2,该分子中的共价键类型为极性共价键和非极性共价键;
(5) S的最高价氧化物对应的水化物的浓溶液为浓硫酸,与Cu反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目