题目内容
将55g铁片放入硫酸铜溶液片刻,取出洗涤干燥后称重,质量为56.6g,求参加反应的铁和生成的铜的质量.
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Fe+CuSO4=FeSO4+Cu,根据固体质量差,利用差量法计算参加反应的铁和生成的铜的质量.
解答:
解:设参加反应的Fe的质量为x,生成Cu的质量为y,则:
Fe+CuSO4=FeSO4+Cu 固体质量增加
56 64 64-56=8
x y 56.6g-55g=1.6g
56:8=x:1.6g,解得x=11.2g
64:8=y:1.6g,解得y=12.8g
答:参加反应的Fe为11.2g,生成的Cu为12.8g.
Fe+CuSO4=FeSO4+Cu 固体质量增加
56 64 64-56=8
x y 56.6g-55g=1.6g
56:8=x:1.6g,解得x=11.2g
64:8=y:1.6g,解得y=12.8g
答:参加反应的Fe为11.2g,生成的Cu为12.8g.
点评:本题考查化学方程式有关计算,难度不大,利用差量法简化计算步骤,注意根据质量守恒定律理解差量法.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列除去杂质的方法错误的是( )
| A、除去SiO2中少量NH4Cl:在空气中充分灼烧 |
| B、除去铜器表面的铜绿[Cu2(OH)2CO3]:用盐酸浸泡,再用清水冲洗 |
| C、除去CO2中混有的少量的HCl:用NaOH溶液洗气,再干燥 |
| D、除去FeCl2溶液中混有的CuCl2:可在溶液中加入铁粉,充分反应后过滤 |
下列各组物质的主要成分,皆为同一种酸所对应的盐是( )
| A、大理石、重晶石、光卤石 |
| B、小苏打、苏打、大苏打 |
| C、绿矾、胆矾、明矾 |
| D、铝土矿、硫铁矿、磁铁矿 |
下列实验中,所加固体可以完全溶解的是( )
| A、在H2O2溶液中加入少量MnO2粉末 |
| B、将一小块铝片投入足量NaOH溶液中 |
| C、将少量氢氧化铝加入足量的浓氨水中 |
| D、常温下将一小块铁片投入足量的浓硝酸中 |
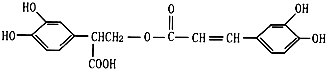
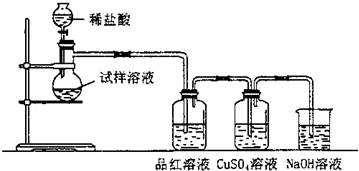
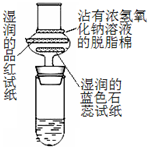 浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2-3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞.可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质--“黑面包”.分析实验效果更加明显的原因:
浓硫酸与蔗糖反应的演示实验装置修改如下:实验时在大试管中先放入2g细小颗粒的蔗糖,滴加2-3滴碳酸钠浓溶液,再加入1.5mL 98%的浓硫酸,迅速塞紧带干燥管的单孔橡皮塞.可以看到,蔗糖迅速变黑,体积急剧膨胀,形成多孔海绵状固体物质--“黑面包”.分析实验效果更加明显的原因: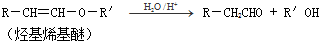
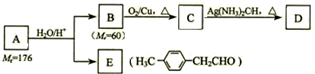
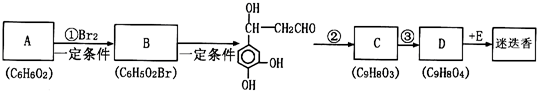
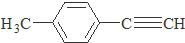 )的一条路线如下:
)的一条路线如下: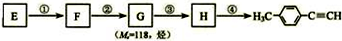
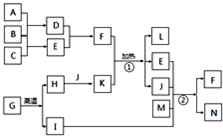 以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.
以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.