题目内容
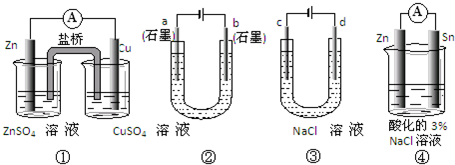
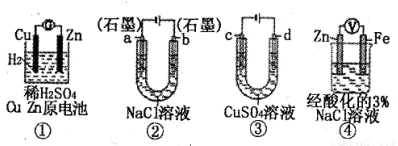
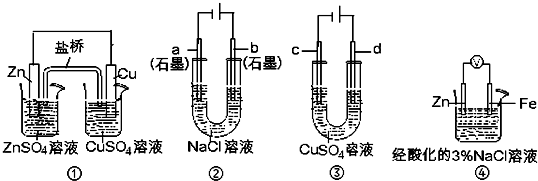
关于下列装置说法正确的是
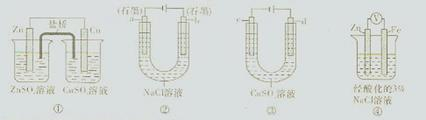
- A.装置①中,盐桥中的K+移向ZnSO4溶液
- B.装置②工作一段时间后,a极附近溶液的pH增大
- C.用装置③精炼铜时,c极为粗铜
- D.装置④中电子由Zn流向Fe,装置中有Fe2+生成
B
试题分析:装置①中锌是负极,铜是正极,原电池中阳离子向正极移动,所以盐桥中的K+移向CuSO4溶液,A不正确;装置②中a电极与电源的负极相连,是阴极,溶液中的氢离子放电,从而破坏a电极附近溶液中水的电离平衡,溶液显碱性,选项B正确;精练铜时粗铜和电源的正极相连,做阳极,装置③中d应该是粗铜,选项C不正确;装置④中锌的活泼性强于铁的,锌是负极,铁是正极,锌失去电子,溶液中的氧气得到电子,D不正确,答案选B。
考点:考查电化学原理的综合应用和判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,紧扣教材,侧重对学生能力的培养,有利于调动学生的学习兴趣和学习积极性。该题的关键是明确原电池和电解池的工作原理,然后结合有关的装置灵活运用、分析、判断姐。
试题分析:装置①中锌是负极,铜是正极,原电池中阳离子向正极移动,所以盐桥中的K+移向CuSO4溶液,A不正确;装置②中a电极与电源的负极相连,是阴极,溶液中的氢离子放电,从而破坏a电极附近溶液中水的电离平衡,溶液显碱性,选项B正确;精练铜时粗铜和电源的正极相连,做阳极,装置③中d应该是粗铜,选项C不正确;装置④中锌的活泼性强于铁的,锌是负极,铁是正极,锌失去电子,溶液中的氧气得到电子,D不正确,答案选B。
考点:考查电化学原理的综合应用和判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,紧扣教材,侧重对学生能力的培养,有利于调动学生的学习兴趣和学习积极性。该题的关键是明确原电池和电解池的工作原理,然后结合有关的装置灵活运用、分析、判断姐。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
关于下列装置说法正确的是( )
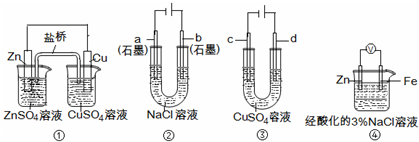

| A、装置①中,盐桥中的K+移向ZnSO4溶液 | B、装置②工作一段时间后,a极附近溶液的pH增大 | C、用装置③精炼铜时,c极为粗铜 | D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
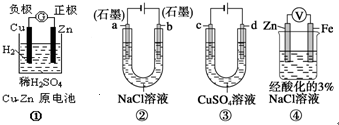 关于下列装置说法正确的是( )
关于下列装置说法正确的是( )