题目内容
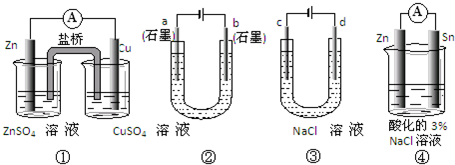
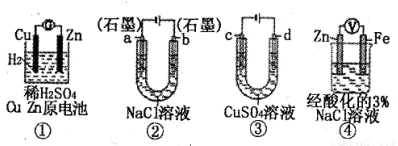
关于下列装置说法正确的是( )
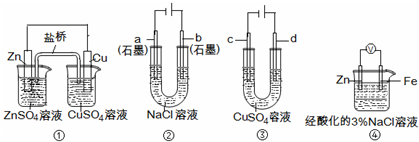

| A、装置①中,盐桥中的K+移向ZnSO4溶液 | B、装置②工作一段时间后,a极附近溶液的pH增大 | C、用装置③精炼铜时,c极为粗铜 | D、装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
分析:A、在原电池中,电解质中的阳离子移向正极;
B、在电解池的阴极上是阳离子发生得电子的还原反应;
C、电解精炼铜时,电解池的阳极是粗铜;
D、在金属的电化学腐蚀中,电子是从负极流向正极,根据电极反应来判断即可.
B、在电解池的阴极上是阳离子发生得电子的还原反应;
C、电解精炼铜时,电解池的阳极是粗铜;
D、在金属的电化学腐蚀中,电子是从负极流向正极,根据电极反应来判断即可.
解答:解:A、在装置①中,金属锌是负极,金属铜是正极,盐桥中的K+移向CuSO4溶液,故A错误;
B、在电解池装置②的阴极上是阳离子氢离子发生得电子的还原反应,氢离子浓度减小,所以a极附近溶液的pH增大,故B正确;
C、电解精炼铜时,电解池的阳极是粗铜,阴极时精铜,即c极为精铜,故C错误;
D、在金属的电化学腐蚀中,金属锌是负极,金属铁是正极,电子是从负极Zn流向正极Fe,装置中铁电极上会产生氢气,故D错误.
故选:B.
B、在电解池装置②的阴极上是阳离子氢离子发生得电子的还原反应,氢离子浓度减小,所以a极附近溶液的pH增大,故B正确;
C、电解精炼铜时,电解池的阳极是粗铜,阴极时精铜,即c极为精铜,故C错误;
D、在金属的电化学腐蚀中,金属锌是负极,金属铁是正极,电子是从负极Zn流向正极Fe,装置中铁电极上会产生氢气,故D错误.
故选:B.
点评:本题考查学生原电池、电解池的工作原理等方面的知识,注意知识的归纳和整理是解题关键,难度不大.

练习册系列答案
相关题目
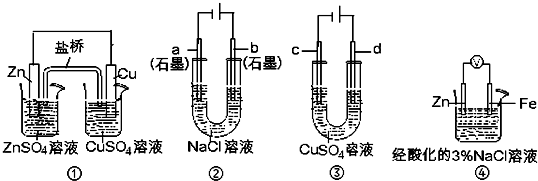
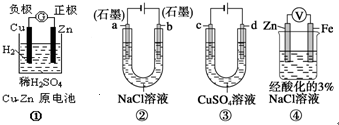 关于下列装置说法正确的是( )
关于下列装置说法正确的是( )