题目内容
20.下列关于甲烷的说法不正确的是( )| A. | 是最简单的有机化合物 | |
| B. | 在1500℃以上能比较完全地分解,生成炭黑和氢气 | |
| C. | 与等物质的量的氯气混合在光照下充分反应,生成物中HC1的物质的量最大 | |
| D. | 完全燃烧生成的CO2和H2O的物质的量之比是1:1 |
分析 A.甲烷分子组成是有机物中最简单的有机化合物;
B.根据甲烷是有碳元素和氢元素组成进行解答;
C.甲烷第一步取代生成等量的HCl和一氯甲烷,在后续的取代中氯代甲烷总的物质的量不变,而HCl不断增多,因此其物质的量在生成物中最大;
D.烃完全燃烧时生成CO2与H2O的物质的量之比为1:1,根据C原子、H原子守恒可知烃分子满足C原子数与H原子数之比为1:2,据此判断.
解答 解:A.甲烷分子组成是有机化合物中最简单的物质,故A正确;
B.甲烷是有碳元素和氢元素组成,隔绝空气将甲烷加热到1000℃以上,甲烷分解生成炭黑和氢气,故B正确;
C.甲烷在发生取代反应时,除了生成有机物之外,还有氯化氢生成,且有几个氢原子,就生成几分子氯化氢,所以氯化氢的量最多,故C正确;
D.CH4中C原子数与H原子数之比为1:4,完全燃烧时生成CO2与H2O的物质的量之比为1:,2,完全燃烧生成的CO2和H2O的物质的量之比是1:1,C原子数与H原子数之比为1:2,故D错误;
故选D.
点评 本题考查了甲烷的性质,为高频考点,题目难度不大,注意甲烷的饱和烃性质以及取代反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.将CO2持续通入下列八种饱和溶液:①Na2CO3 ②Na2SiO3 ③NaAlO2 ④C6H5ONa ⑤Ca(ClO)2 ⑥CaCl2 ⑦NH3和NaCl ⑧Ca(OH)2,最终能得到沉淀、浊液或析出晶体的是( )
| A. | ②⑤⑧ | B. | ⑤⑥⑧ | C. | ①②③④⑦ | D. | ②③④⑧ |
11.六氟化硫(SF6)具有良好的高压绝缘性,在电器工业中有着广泛的用途,SF6分子呈正八面体结构,S 原子位于正八面体的中心.下列关于SF6的推测中,正确的是( )
| A. | SF6在氧气中燃烧可生成SO2 | |
| B. | SF6晶体是原子晶体 | |
| C. | SF6是非极性分子 | |
| D. | SF6中各原子的最外电子层都达到8电子稳定结构 |
8.下列有关化学反应速率和限度的说法中,正确的是( )
| A. | 用H2O2分解制O2,加入1~2滴FeCl3溶液,反应速率加快 | |
| B. | 在金属钠与足量水反应中,增加水的量能加快反应速率 | |
| C. | 一定条件下的反应:2SO2+O2?2SO3中,SO2的转化率能达到100% | |
| D. | 用铁和稀硫酸制取氢气,将稀硫酸换成浓硫酸可以加快反应速率 |
15.下列实验装置或操作能达到实验目的是( )
| A. | 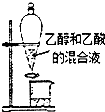 分离乙醇和乙酸 | B. |  制取乙酸乙酯 制取乙酸乙酯 | C. | 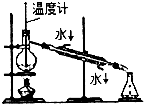 石油的蒸馏 石油的蒸馏 | D. | 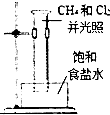 甲烷与氯气反应 |
5. 用6g CaCO3与100mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如图所示.下列说法正确的是( )
用6g CaCO3与100mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如图所示.下列说法正确的是( )
 用6g CaCO3与100mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如图所示.下列说法正确的是( )
用6g CaCO3与100mL稀盐酸反应制取少量的CO2,反应过程中生成的CO2的体积(已折算为标准状况)随反应时间变化的情况如图所示.下列说法正确的是( )| A. | OE段表示的平均反应速率最快,可能的原因是该反应是放热反应 | |
| B. | EF段用HC1浓度的减小表示的该反应的平均反应速率为0.2 mol/(L•min) | |
| C. | 在F点收集到的CO2的体积最大 | |
| D. | 在G点以后收集的CO2的量不再增多,原因是稀盐酸已反应完全 |
12.分析原子的杂化方式,并根据等电子体原理判断下列各组分子中的所有原子,或者处于同一平面,或者在一条直线上的是( )
| A. | C2H2、HClO、C2H6 | B. | CO2、N2O、HC≡C-NH2 | ||
| C. | C6H5CH3、C3H4、CH4 | D. | C6H6、C2H4、HCN |
9.下列化学反应,属于取代反应的是①由乙酸制乙酸乙酯 ②油脂的皂化反应制肥皂③由乙烯与水反应制乙醇 ④苯与硝酸反应制硝基苯( )
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |