题目内容
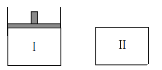
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是

A. 元素W的最高价氧化物对应水化物的酸性比Q的强
B. 离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+)
C. 元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键
D. X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
【答案】A
【解析】试题解析:根据题意:Q为氯;W 硫 Y氧 X氮、Z铝 ;A.硫酸的酸性小于高氯酸;A错误;B.电子层结构相同的离子,核电核数越大,离子半径越小;r(S2-)>r(Cl-)>r(O2-)>r(Al3+); B正确;C.氨气和氯化氢反应生成氯化铵,既含共价键又含离子键;C正确;D.五氧化二氮、氧化铝、三氧化硫、高氯酸均能与强碱反应;D正确;
考点:元素周期表知识。

 黄冈创优卷系列答案
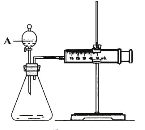
黄冈创优卷系列答案【题目】用如下图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7克镁带,按右图连接好装置,从A中加入20.0ml0.5mol/LH2SO4。记录注射器活塞的位置和相应的时间。记录数据如下
时间/s | 0 | t | 2t | ...... |
活塞的位置/ml | 17.3 | 25.6 | 36.6 | ...... |
(1)检查该装置气密性的方法是。
(2)仪器A的名称是。
(3)0-t时间段与t-2t时间段,化学反应速率最快的是,原因是。
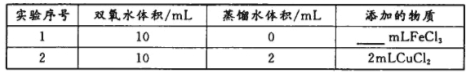
(4)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0.1mol/LFeCl3、0.2mol/LCuCl2,完成下表的实验设计:
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:___________。
②上表中需要添加的物质是mlFeCl3溶液。
③本实验需要测定的数据是。
(5)为确定MnO2催化双氧水分解的最佳条件,用该实验装置进行实验,反应物用量和反应停止的时间数据如下表。
MnO2 时间 H2O2 | 0.1g | 0.3g | 0.8g |
10mL1.5% | 223s | 67s | 36s |
10mL3.0% | 308s | 109s | 98s |
10mL4.5% | 395s | 149s | 116s |
分析表中数据回答下列问题:
①相同浓度的过氧化氢的分解速率随着MnO2用量的增加而_______(填“加快”、“减慢”或“不变”)。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入__________g的MnO2为较佳选择。
③该小组的某同学分析上述数据后认为:“当用相同质量的MnO2时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确?______(填“正确”或“不正确”),理由是_________________________。(提示:H2O2溶液的密度可认为近似相等。)