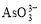题目内容
实验室用标准盐酸测定未知浓度NaOH溶液,用甲基橙作指示剂,下列操作可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准酸液润洗
B.开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失
C.锥形瓶内溶液颜色由黄变橙时立即停止滴定
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
C
【解析】
试题分析:根据c(NaOH)=c(HCl)×V(HCl)/V(NaOH)判断。A、酸式滴定管在装酸液前未用标准酸液润洗,标准液被稀释,所用标准液的体积偏大,测定结果偏高,错误;B、开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失,所用标准液的体积偏大,测定结果偏高,错误;C、锥形瓶内溶液颜色由黄变橙时立即停止滴定,所用标准液的体积偏小,测定结果偏低,正确;D、盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次,所用标准液的体积偏大,测定结果偏高,错误。
考点:考查酸碱中和滴定误差分析。

已知25℃时部分弱电解质的电离平衡常数数据如表所示:
化学式 | CH3COOH | H2CO3 | HClO | |
电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液;a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是_______________(用编号填写)。
(2)常温下,0.1mol·L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
A.c(H+ )
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-)
D.c(OH-)/c(H+)
E.c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如下图所示,则同温度时HX的电离平衡常数_ ____(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是_____________________。

(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精确值)。
(5)标准状况下,将1.12L CO2通入100mL 0.75mol·L-1的NaOH溶液中,则溶液中离子的浓度由大到小的顺序