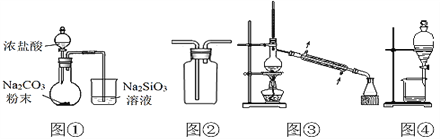
ЬтФПФкШн
ЁОЬтФПЁПЯТБэЪЧ25ЁцЪБФГаЉбЮЕФШмЖШЛ§ГЃЪ§КЭШѕЫсЕФЕчРыЦНКтГЃЪ§ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
ЛЏбЇЪН | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
KaЛђKsp | Ka=1.8ЁС10-5 | Ka1=4.1ЁС10-7 Ka2=5.6ЁС10-11 | Ksp=1.8ЁС10-10 | Ksp=2.0ЁС10-12 |
A. ГЃЮТЯТЃЌЯрЭЌХЈЖШЂйCH3COONH4 ЂкNH4HCO3 ЂлЃЈNH4ЃЉ2CO3ШмвКжаЃЌcЃЈNH4+ЃЉгЩДѓЕНаЁЕФЫГађЪЧЃКЂйЃОЂкЃОЂл
B. AgCl взШмгкАБЫЎФбШмгкЫЎЃЌЫљвдAgCl дкАБЫЎжаЕФKsp ДѓгкЫЎжаЕФ Ksp
C. ЯђБЅКЭТШЫЎжаЕЮМгNaOH ШмвКжСШмвКИеКУЮЊжаадЪБЃЌcЃЈNa+ЃЉ=2cЃЈClO-ЃЉ+cЃЈHClOЃЉ
D. ЯђХЈЖШОљЮЊ1ЁС10-3molL-1ЕФKCl КЭK2CrO4ЛьКЯвКжаЕЮМг1ЁС10-3molL-1 ЕФAgNO3ШмвКЃЌCrO42-ЯШаЮГЩГСЕэ
ЁОД№АИЁПC
ЁОНтЮіЁПAЃЎЕчРыГЃЪ§дНДѓЃЌЫсаддНЧПЃЌгЩЭМЫсадЃКCH3COOHЃОH2CO3ЃОHCO3-ЃЛЫсаддНШѕЃЌЖдгІЕФЫсИљРызгЫЎНтФмСІдНЧПЃЌдђЫЎНтФмСІЃКCH3COO-ЃМHCO3-ЃМCO32-ЃЌДзЫсИљРызгЁЂЬМЫсЧтИљРызгКЭЬМЫсИљРызгДйНјяЇИљРызгЫЎНтЃЌШѕЫсИљРызгЫЎНтГЬЖШдНДѓЃЌдђяЇИљРызгЫЎНтГЬЖШдНДѓЃЌЕЋ(NH4)2CO3ШмвКжа(NH4+)ЕФСПЪЧCH 3COONH4ЁЂNH4HCO3ЕФСНБЖЃЌЫЎНтЪЧМЋЦфЮЂШѕЕФЃЌЫљвд(NH4)2CO3жаc(NH4+)зюДѓЃЌгІЮЊЂлЃОЂйЃОЂкЃЌЙЪAДэЮѓЃЛBЃЎAgCl взШмгкАБЫЎФбШмгкЫЎЃЌЫЕУїAgCl дкАБЫЎжаЕФШмНтЖШДѓгкЫЎжаЕФШмНтЖШЃЌЙЪBДэЮѓЃЛCЃЎЯђБЅКЭТШЫЎжаЕЮМгNaOHШмвКЃЌИљОнЕчКЩЪиКугаЃКc(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-)ЃЌЫљвдc(Na+)=c(Cl-)+c(ClO-)ЃЌШмвКГЪжаадЃЌдђc(H+)=c(OH-)ЃЌЫљвдc(Na+)=c(Cl-)+c(ClO-)ЃЌИљОнЮяСЯЪиКуЕУЃКc(Cl-)=c(ClO-)+c(HClO)ЃЌЖўепНсКЯПЩЕУЃКc(Na+)=c(HClO)+2c(ClO-)ЃЌЙЪCе§ШЗЃЛDЃЎAgClБЅКЭЫљашAg+ХЈЖШc(Ag+)=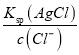 =
=![]() =1.8ЁС10-7ЃЌAg2CrO4БЅКЭЫљашAg+ХЈЖШc(Ag+)=
=1.8ЁС10-7ЃЌAg2CrO4БЅКЭЫљашAg+ХЈЖШc(Ag+)=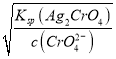 =
=![]() =4.472ЁС10-5ЃЌ1.8ЁС10-7ЃМ4.472ЁС10-5ЃЌЫљвдCl-ЯШГСЕэЃЌЙЪDДэЮѓЃЛЙЪД№АИЮЊCЁЃ
=4.472ЁС10-5ЃЌ1.8ЁС10-7ЃМ4.472ЁС10-5ЃЌЫљвдCl-ЯШГСЕэЃЌЙЪDДэЮѓЃЛЙЪД№АИЮЊCЁЃ