题目内容
某化学兴趣小组用含铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下图所示:
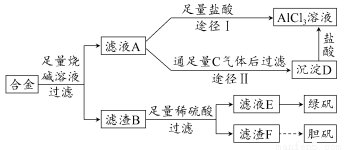
试回答下列问题:
(1)过滤时用的器材已有:滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是________。
(2)由滤液A制AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是________,理由是_____________________________。
(3)从滤液E中得到绿矾晶体的实验操作是________。
(4)写出用滤渣F制备胆矾晶体的化学方程式_______________________。
(5)有同学提出可将方案中最初用于溶解合金的烧碱改为盐酸,重新设计方案,也能制得这三种物质,你认为后者的方案是否合理?________,理由是________________________________________________。
(1)漏斗、玻璃棒
(2)途径Ⅱ 因为滤液A是NaAlO2溶液,按途径Ⅰ直接向A加入盐酸得到的AlCl3中含有大量的NaCl杂质;按途径Ⅱ通入C(CO2)气体,得到D[Al(OH)3]沉淀,将Al(OH)3溶于盐酸中得到的是纯净的AlCl3溶液,所以途径Ⅱ更合理
(3)蒸发浓缩,冷却结晶
(4)2Cu+O2 2CuO
2CuO
CuO+H2SO4=CuSO4+H2O
CuSO4+5H2O=CuSO4·5H2O
(5)不合理 该方案不符合实验方案设计的简约性原则,操作步骤多,消耗试剂量大,时间长
【解析】(1)过滤需要漏斗、玻璃棒。(2)制AlCl3溶液途径Ⅱ合理,因为滤液A是NaAlO2溶液,加足量盐酸会生成NaCl杂质。(3)绿矾是FeSO4·7H2O,需浓溶液冷却结晶才能含结晶水。(4)需三步反应:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O,CuSO4+5H2O=CuSO4·5H2O,(5)先用盐酸溶解会步骤多,且浪费药品。
2CuO,CuO+H2SO4=CuSO4+H2O,CuSO4+5H2O=CuSO4·5H2O,(5)先用盐酸溶解会步骤多,且浪费药品。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案