题目内容
11.用x射线衍射法可以测得阿伏加德罗常数.对金属铜的测定结果为:晶胞为面心立方最密堆积,铜原子直径为dpm,又知铜的密度为bg•cm-3,则阿伏加德罗常数NA=$\frac{64\sqrt{2}}{b{d}^{3}}×1{0}^{30}$mol-1.分析 晶胞为面心立方最密堆积,则晶胞的面对角线为铜原子半径的4倍,铜原子直径为dpm,则晶胞的边长为$\frac{2d}{\sqrt{2}}$pm,所以晶胞的体积为($\frac{2d}{\sqrt{2}}$×10-10cm)3,所以晶胞的质量为bg•cm-3×($\frac{2d}{\sqrt{2}}$×10-10cm)3,铜的摩尔质量=$\frac{1}{4}$×晶胞质量×NA,据此计算NA.
解答 解:晶胞为面心立方最密堆积,则晶胞的面对角线为铜原子半径的4倍,铜原子直径为dpm,则晶胞的边长为$\frac{2d}{\sqrt{2}}$pm,所以晶胞的体积为($\frac{2d}{\sqrt{2}}$×10-10cm)3,所以晶胞的质量为bg•cm-3×($\frac{2d}{\sqrt{2}}$×10-10cm)3=$2\sqrt{2}b{d}^{3}×1{0}^{-30}$g,铜的摩尔质量=$\frac{1}{4}$×晶胞质量×NA,所以NA=$\frac{4×64}{2\sqrt{2}b{d}^{3}×1{0}^{-30}}$mol-1=$\frac{64\sqrt{2}}{b{d}^{3}}×1{0}^{30}$mol-1,
故答案为:$\frac{64\sqrt{2}}{b{d}^{3}}×1{0}^{30}$.
点评 本题综合考查物质的结构与性质知识,侧重于晶胞的结构与NA的计算,题目难度中等,注意把握基本公式的运算.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
1.已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)?CO2(g)+H2(g)
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:T℃时物质的浓度(mol/L)变化
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的.第4~5min之间,改变的条件是增大氢气的浓度,C2>0.104 (填“>”、“=”、“<”).T℃时该化学反应的平衡常数是0.5.
②已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 是多少?(请写出计算过程,无过程结果不给分)
③397℃时该反应的平衡常数为12,请判断该反应的△H<0 (填“>”、“=”、“<”).
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:T℃时物质的浓度(mol/L)变化
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
②已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 是多少?(请写出计算过程,无过程结果不给分)
③397℃时该反应的平衡常数为12,请判断该反应的△H<0 (填“>”、“=”、“<”).
6.NA代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 11.2L氧气所含原子数是NA | |
| B. | 80g硝酸铵所含氮原子数是2NA | |
| C. | 1 mol 氦气所含氦原子数是2NA | |
| D. | 1L1mol/L的盐酸溶液中所含氯化氢分子数是NA |
20.下列物质的分子组成不符合通式CnH2n-6的是( )
| A. |  | B. |  | C. | 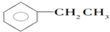 | D. | 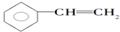 |
1.在同温同压下,一定量的某有机物和过量的金属钠反应产生aL氢气,另取等量的该有机物与足量的小苏打溶液反应,可以收集二氧化碳气体bL,若a=b,则该有机物可能是( )
| A. | HOOC-CH2-CH2OH | B. | HOOC-CH2-COOH | C. | HOCH2-CH2-CH2OH | D. | CH3-CH2-COOH |