题目内容
10.如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列分析正确的是( )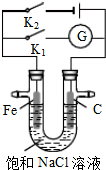
| A. | K1闭合,铁棒上发生的反应为2H++2e-→H2↑ | |
| B. | K1闭合,石墨棒周围溶液pH逐渐降低 | |
| C. | K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法 | |
| D. | K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体 |
分析 若闭合K1,该装置没有外接电源,所以构成了原电池;组成原电池时,较活泼的金属铁作负极,负极上铁失电子发生氧化反应;石墨棒作正极,正极上氧气得电子生成氢氧根离子发生还原反应;若闭合K2,该装置有外接电源,所以构成了电解池,Fe与负极相连为阴极,碳棒与正极相连为阳极,据此判断.
解答 解:A、若闭合K1,该装置没有外接电源,所以构成了原电池,较活泼的金属铁作负极,负极上铁失电子,Fe-2e-=Fe2+,故A错误;
B、若闭合K1,该装置没有外接电源,所以构成了原电池;不活泼的石墨棒作正极,正极上氧气得电子生成氢氧根离子发生还原反应,电极反应式为2H2O+O2+4e-=4OH-,所以石墨棒周围溶液pH逐渐升高,故B错误;
C、K2闭合,Fe与负极相连为阴极,铁棒不会被腐蚀,属于外加电源的阴极保护法,故C正确;
D、K2闭合,电路中通过0.4NA个电子时,阴极生成0.2mol氢气,阳极生成0.2mol氯气,两极共产生0.4mol气体,状况不知无法求体积,故D错误.
故选C.
点评 本题考查了原电池原理和电解池原理,能正确判断电池的类型及两极的反应是解本题的关键,题目难度中等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
1.已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)?CO2(g)+H2(g)
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:T℃时物质的浓度(mol/L)变化
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的.第4~5min之间,改变的条件是增大氢气的浓度,C2>0.104 (填“>”、“=”、“<”).T℃时该化学反应的平衡常数是0.5.
②已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 是多少?(请写出计算过程,无过程结果不给分)
③397℃时该反应的平衡常数为12,请判断该反应的△H<0 (填“>”、“=”、“<”).
①T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:T℃时物质的浓度(mol/L)变化
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
②已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 是多少?(请写出计算过程,无过程结果不给分)
③397℃时该反应的平衡常数为12,请判断该反应的△H<0 (填“>”、“=”、“<”).
20.下列物质的分子组成不符合通式CnH2n-6的是( )
| A. |  | B. |  | C. | 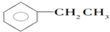 | D. | 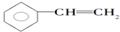 |
 2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂.请回答下列问题:
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂.请回答下列问题: (1)已知:O2 (g)═O2+ (g)+e-△H1=+1175.7kJ•mol-1
(1)已知:O2 (g)═O2+ (g)+e-△H1=+1175.7kJ•mol-1 对如图中两极进行必要的连接并填空:
对如图中两极进行必要的连接并填空: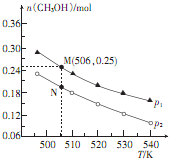 以天然气为原料合成甲醇常见的方法有水煤气和目前正在开发的直接氧化法
以天然气为原料合成甲醇常见的方法有水煤气和目前正在开发的直接氧化法