题目内容
(13分)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)Y基态原子的电子排布式是________;Z所在周期中第一电离能最大的主族元素是_____。
(2)XY2-离子的立体构型是_______;R2+的水合离子中,提供孤电子对的是原子是______。
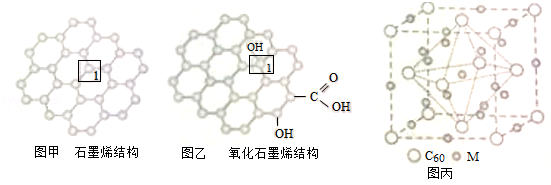
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数之比是___________。

(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________。
(1)Y基态原子的电子排布式是________;Z所在周期中第一电离能最大的主族元素是_____。
(2)XY2-离子的立体构型是_______;R2+的水合离子中,提供孤电子对的是原子是______。
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数之比是___________。

(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________。
(1)1s22s22p4;Cl (2)V形;O (3)2:1
(4)2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
(4)2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
试题分析:X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体,该气体是NO2,则X是氮元素,Y是氧元素;X与氢元素可形成XH3,该气体是氨气;Z基态原子的M层与K层电子数相等,则该元素的原子序数是2+8+2=12,即为镁元素;R2+离子的3d轨道中有9个电子,因此R的原子序数是18+9+2=29,即为铜元素。
(1)氧元素的原子序数是8,则根据核外电子排布规律可知,氧元素基态原子的电子排布式是1s22s22p4;同周期自左向右元素的第一电离能逐渐增大,镁是第三周期,则所在周期中第一电离能最大的主族元素是Cl元素。
(2)根据价层电子对互斥理论可知,NO2-离子中心原子氮原子含有的孤对电子对数=
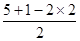 =1,即氮原子的价层电子对数是3,由于含有一对孤对电子,因此其离子的立体构型是V形;铜离子含有空轨道,而水分子中的氧原子含有孤对电子,因此在Cu2+的水合离子中,提供孤电子对的是原子是O原子。
=1,即氮原子的价层电子对数是3,由于含有一对孤对电子,因此其离子的立体构型是V形;铜离子含有空轨道,而水分子中的氧原子含有孤对电子,因此在Cu2+的水合离子中,提供孤电子对的是原子是O原子。(3)根据晶胞结构可知,阳离子在8个顶点和体心处各一个,则根据均摊法可知,阳离子个数=1+8×
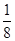 =2个。阴离子在上下面各2个,晶胞内部2个,则阴离子个数=4×
=2个。阴离子在上下面各2个,晶胞内部2个,则阴离子个数=4×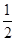 +2=4个,因此晶胞中阴离子与阳离子的个数之比是4:2=2:1。
+2=4个,因此晶胞中阴离子与阳离子的个数之比是4:2=2:1。(4)将R单质的粉末加入氨气的浓溶液中,通入氧气,充分反应后溶液呈深蓝色,这说明在反应中铜被氧化氧化为铜离子与氨气结合形成配位键,则该反应的离子方程式是2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O。

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目