��Ŀ����
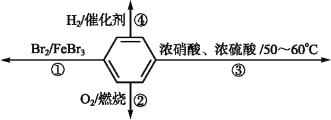
����Ŀ����֪A������ʯ�͵���Ҫ�л�����ԭ�ϣ�E�Ǿ��й���ζ���л��F��һ�ָ߾�����Ƴɶ��ְ�װ���ϡ�������ͼת����ϵ������и��⣺
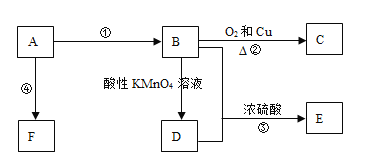
��1��A�ķ���ʽ��__��C��������__��F�Ľṹ��ʽ��__��
��2��D�����еĹ�����������__�������һ����ʵ������֤D���ʴ��ڸù����ţ��䷽����__��
��3��д����Ӧ�ڵĻ�ѧ����ʽ��ָ���۵ķ�Ӧ���ͣ�
��Ӧ�ڣ�__����Ӧ��������__��Ӧ��
���𰸡�C2H4 ��ȩ ![]() �Ȼ� ��D�еμ���NaHCO3��Һ������ɫʯ���Լ������������ݲ���������Һ��죩�������Ȼ������� 2C2H5OH+O2
�Ȼ� ��D�еμ���NaHCO3��Һ������ɫʯ���Լ������������ݲ���������Һ��죩�������Ȼ������� 2C2H5OH+O2![]() 2CH3CHO+2H2O ��������ȡ����
2CH3CHO+2H2O ��������ȡ����
��������
A������ʯ�͵���Ҫ�л�����ԭ�ϣ�A�õ���F��һ�ָ߾�����Ƴɶ��ְ�װ���ϣ���AΪCH2=CH2��CH2=CH2�����Ӿ۷�Ӧ���ɸ߾���FΪ![]() ��B��������������C�������Ը��������Һ����D����BΪ����CΪȩ��DΪ���ᣬ��CH2=CH2��ˮ�����ӳɷ�Ӧ����BΪCH3CH2OH��CH3CH2OH��������������CΪCH3CHO��B��������DΪCH3COOH��CH3COOH��CH3CH2OH����������Ӧ����EΪCH3COOCH2CH3���ݴ˷������
��B��������������C�������Ը��������Һ����D����BΪ����CΪȩ��DΪ���ᣬ��CH2=CH2��ˮ�����ӳɷ�Ӧ����BΪCH3CH2OH��CH3CH2OH��������������CΪCH3CHO��B��������DΪCH3COOH��CH3COOH��CH3CH2OH����������Ӧ����EΪCH3COOCH2CH3���ݴ˷������
��1��AΪ��ϩ������ʽΪC2H4��C����ȩ��F�ṹ��ʽΪ![]() ���ʴ�Ϊ��C2H4����ȩ��
���ʴ�Ϊ��C2H4����ȩ��![]() ��
��
��2��DΪCH3COOH���������������Ȼ����Ȼ��ܺ�̼�����Ʒ�Ӧ���ɶ�����̼����ʹ��ɫʯ����Һ���ɫ������鷽��Ϊ��D�еμ���NaHCO3��Һ������ɫʯ���Լ������������ݲ���������Һ��죩�������Ȼ������ţ����������������ɣ����ʴ�Ϊ���Ȼ�����D�еμ���NaHCO3��Һ������ɫʯ���Լ������������ݲ���������Һ��죩�������Ȼ������ţ�
��3���������Ҵ��Ĵ�������Ӧ����Ӧ����ʽΪ2C2H5OH+O2![]() 2CH3CHO+2H2O���÷�Ӧ��������Ҵ���������Ӧ����Ӧ������������Ӧ��ȡ����Ӧ���ʴ�Ϊ��2C2H5OH+O2
2CH3CHO+2H2O���÷�Ӧ��������Ҵ���������Ӧ����Ӧ������������Ӧ��ȡ����Ӧ���ʴ�Ϊ��2C2H5OH+O2![]() 2CH3CHO+2H2O����������ȡ������
2CH3CHO+2H2O����������ȡ������

����Ŀ���±�ΪԪ�����ڱ���һ���֣��û�ѧ����ش��������⣺
���� ���� | I | II | III | IV | V | VI | VII |
һ | �� | ||||||
�� | �� | �� | �� | ||||
�� | �� | �� | �� | �� | �� | �� |
(1)���ԭ�ӽṹʾ��ͼΪ________________��
(2)�ܺ͢������ڱ��е�λ�÷ֱ���________________��________________��
(3)�ں͢���̬�⻯���ȶ��ԵĴ�С˳��________________(�ѧʽ)��
(4)�ۢ�����ۺ������������ǿ����________________(�ѧʽ)��
(5)�۵���̬�⻯����۵�����������Ӧ��ˮ���ﷴӦ���ɵ�����__(�ѧʽ)������___(�������ۻ��������������ӻ�������)��
(6)�٢ܢ�����Ԫ�ص�ԭ�����γ�ԭ����Ŀ��Ϊ1��1��1�Ĺ��ۻ�������ĵ���ʽΪ_____��
(7)���ȽϢܺ͢�����Ԫ�صķǽ�����ǿ����������Ϊ��֤��֤����_____(����ĸ)��
A���Ƚ�������Ԫ�ص��ʵķе�
B���Ƚ�������Ԫ�ص������������ϵ���
C���Ƚ�������Ԫ�ص�����������Ӧˮ����������
D���Ƚ�������Ԫ�ص��������Ӧ��������
����Ŀ������ʵ�鷽�������ﵽ��ӦĿ�ĵ���
A | B | C | D | |
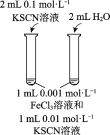
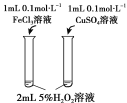
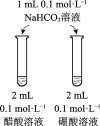
Ŀ�� | �Ƚ�̼�����̼�����ˮ��̶� | �о�Ũ�ȶԻ�ѧƽ���Ӱ�� | �Ƚϲ�ͬ�����Ի�ѧ��Ӧ���ʵ�Ӱ�� | �Ƚ�̼�ᡢ��������������ǿ�� |
ʵ�鷽�� |
|
|
|
|
A. AB. BC. CD. D