题目内容
【题目】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于_______区,单质X的晶体类型为____________,其中X原子的配位数为______________。
(2)已知元素Y可与元素Z的相对原子质量只差为16,则元素Y基态原子的外围电子排布图为______________________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是________(写化学式),该酸根离子的立体构型为________。
(3)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为______________________。
(4)X与Y形成的一种化合物的立方晶胞如图所示。
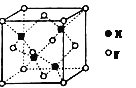
该化合物的化学式为_______,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是______cm。(写出计算式,不要求计算结果。)
【答案】 ds 金属晶体 12 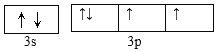 Ar H2SO4 正四面体形 16NA CuS
Ar H2SO4 正四面体形 16NA CuS 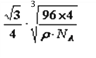
【解析】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,则X的原子序数=2+8+18+1=29,为Cu元素。元素Y基态原子的3p轨道上有2个未成对电子,则Y为硅或硫元素。元素Z 的原子最外层电子数是其内层的3倍,则Z为O元素。
(1)Cu元素在元素周期表中位于ds区,单质铜为金属晶体,铜原子形成晶体时采用的堆积方式为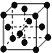 ,其中铜原子的配位数为12,故答案为:ds;金属晶体;12;
,其中铜原子的配位数为12,故答案为:ds;金属晶体;12;
(2)根据上述分析,Y为硅或硫元素,元素Y可与元素Z的相对原子质量只差为16,则元素Y为S,基态原子的外围电子排布图为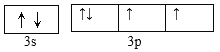 ,第3周期中,第一电离能最大的是Ar。S元素的含氧酸中,酸性最强的是硫酸,SO42-中S的价层电子对数目=4+
,第3周期中,第一电离能最大的是Ar。S元素的含氧酸中,酸性最强的是硫酸,SO42-中S的价层电子对数目=4+![]() (6+2-2×4)=4,采用sp3杂化,立体构型为正四面体形,故答案为:
(6+2-2×4)=4,采用sp3杂化,立体构型为正四面体形,故答案为: ;Ar ;H2SO4;正四面体形;
;Ar ;H2SO4;正四面体形;
(3)氯化铜与氨水反应可形成配合物[Cu(NH3)4]Cl2,1mol该配合物中含有12molN-H,键和4mol配位键,共16mol共价键,σ键的数目为16NA,故答案为:16NA;
(4)依据晶胞结构,利用切割法分析,每个晶胞中含有铜原子个数为:8×![]() +6×
+6×![]() =4,硫原子个数为4,则化学式为;CuS;1mol晶胞中含有4molCuS,1mol晶胞的质量为M(CuS)×4,设晶胞参数为a,则晶体密度ρg·cm–3=
=4,硫原子个数为4,则化学式为;CuS;1mol晶胞中含有4molCuS,1mol晶胞的质量为M(CuS)×4,设晶胞参数为a,则晶体密度ρg·cm–3=![]() =
=![]() ,解得a=
,解得a=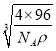 cm,则此晶胞中X与Y的最近距离为体对角线的
cm,则此晶胞中X与Y的最近距离为体对角线的![]() =
=![]() ×
×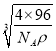 cm,故答案为:CuS;
cm,故答案为:CuS; ![]() ×
×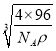 。
。

 口算能手系列答案
口算能手系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________,该分子是__________(填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 | o | p | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
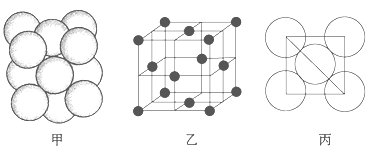
请问晶胞中i原子的配位数为________,一个晶胞中i原子的数目为________。
【题目】化学与生产、生活密切相关,下列对应关系正确的是
选项 | 性质 | 实际应用 |
A | 活性炭可吸附水中的悬浮物 | 用于自来水的杀菌消毒 |
B | SO2具有还原性 | 漂白纸浆 |
C | 铁被氧气氧化时会放出热量 | 铁、活性炭、无机盐、水等的混合物制成暧宝贴 |
D | 氧化铝是两性氧化物 | 作耐高温材料 |
A. A B. B C. C D. D