题目内容
【题目】下列关于胶体和溶液的说法中,正确的是
A.许多胶体能进行电泳是因为这些胶体带电
B.布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
【答案】C
【解析】
试题A、胶体本身不带电,胶粒带电,错误。B.物质在永不停息地作无规则的运动,胶体粒子一直在作无规则的运动,也能发生布朗运动,错误。C.光线透过胶体时,胶体发生丁达尔效应,是胶体的特性,正确。D.饱和氯化铁溶液与稀氢氧化钠溶液反应生成氢氧化铁沉淀,不是胶体,错误。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A(g)+2B(g) ![]() 3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
浓度/ mol·Lˉ1 时间/min | c(A) | c(B) | c(C) |
0 | 1.0 | 1.2 | 0 |
2 | 0.8 | ||
4 | 0.6 | ||
6 | 0.9 |
A.0~2 min内,B的反应速率为0.1 mol·Lˉ1·minˉ1
B.2 min时,C的物质的量浓度为0.4 mol·Lˉ1
C.4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6 min内,容器内气体分子的总物质的量不变
【题目】氢能是一种极具发展潜力的清洁能源,CH4—H2O催化重整是目前大规模制取氢气的重要方法。
(1)CH4-H2O催化重整:
反应Ⅰ:CH4(g)+H2O(g)![]() CO(g)+3H2(g) H1 = +210kJ/mol
CO(g)+3H2(g) H1 = +210kJ/mol
反应Ⅱ: CO(g)+ H2O(g)![]() CO2(g)+H2(g) H2 =﹣41kJ/mol
CO2(g)+H2(g) H2 =﹣41kJ/mol
①提高CH4平衡转化率的条件是________。
a.增大压强 b.加入催化剂 c.增大水蒸气浓度
②CH4、H2O催化重整生成CO2、H2的热化学方程式是________。
③在密闭容器中,将2.0 mol CO与8.0 mol H2O混合加热到800℃发生反应Ⅱ,达到平衡时CO的转化率是80%,其平衡常数为 _________。
(2)实验发现,其他条件不变,相同时间内,向催化重整体系中投入一定量的CaO可以明显提高H2的百分含量。做对比实验,结果如下图所示:
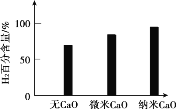
①投入CaO时,H2百分含量增大的原因是:_________。
②投入纳米CaO时,H2百分含量增大的原因是:__________。
(3)反应中催化剂活性会因积炭反应而降低,相关数据如下表:
反应 | Ⅰ | Ⅱ |
|
| |
H(kJ/mol) | +75 | ﹣173 |
①研究发现,如果反应Ⅰ不发生积炭过程,则反应Ⅱ也不会发生积炭过程。因此,若保持催化剂的活性,应采取的条件是_________。
②如果Ⅰ、Ⅱ均发生了积炭反应,通入过量水蒸气能有效清除积炭,反应的化学方程式是_________。