题目内容
某温度下,在体积一定的密闭容器中发生如下反应:2M(g)+N(g) 2E(g)若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%; 若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为( )
2E(g)若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%; 若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为( )
 2E(g)若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%; 若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为( )
2E(g)若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%; 若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为( )| A.20% | B.40% | C.60% | D.80% |
C
试题分析:通过化学反应式中的化学计量数对2molM和1molN“一边倒”是2molE,与开始时的情况呈等效平衡。设达到化学平衡时N转化的物质的量为nmol,则
2M(g)+N(g)
 2E(g)
2E(g)开始的物质的量 2 1 0
转化的物质的量 2n n 2n
平衡的物质的量 2-2n 1-n 2n
根据压强之比等于物质的量之比,即(2-2n+1+n+2n)/3=1+20% 解得n=0.6,M转化的量为1.2mol,转户率为(1.2/2)*100%=60%,故选C。
点评:本题为等效平衡问题,解决这类问题时注意以下两个方面的问题:
(1)对于两边气体分子数不相等的可逆反应,只改变起始时加入物质的物质的量,如果通过可逆反应的化学计量数换算成方程式同一半边的物质时物质的量与起始所给物质对应相同,则两平衡等效.
(2)对于反应前后气体分子数相等的可逆反应,只要反应物(或生成物)的物质的量的比例与起始所给物质的比例对应相同,则两平衡等效。

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
 3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。 B(g)+C(g)。当物质A的起始浓度为1.0 mol·L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示:
B(g)+C(g)。当物质A的起始浓度为1.0 mol·L-1、物质B、C的起始浓度为0时,物质A的浓度、转化率以及物质B的浓度随反应时间的变化如下列各图所示: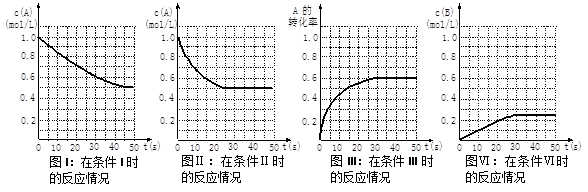
 cZ(g) + dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是
cZ(g) + dW(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的1/2,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是 2C(g)+2D(g);ΔH=Q,2 min末达到平衡,生成0.8 mol D.
2C(g)+2D(g);ΔH=Q,2 min末达到平衡,生成0.8 mol D. mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________ mol.
mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________ mol. 2Y(g) + Z(g),生成物Z 在反应混合物中的体积分数(ψ)与反应时间(t)的关系图正确的是( )
2Y(g) + Z(g),生成物Z 在反应混合物中的体积分数(ψ)与反应时间(t)的关系图正确的是( )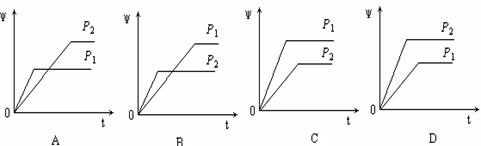
 H++A-,回答下列问题:
H++A-,回答下列问题: Z(g)+2W(g),△H<0。达到平衡时V(A)=1.2aL。试回答:
Z(g)+2W(g),△H<0。达到平衡时V(A)=1.2aL。试回答: