题目内容
用铝热法还原下列化合物,制得金属各1 mol时,消耗铝最少的是( )。
| A.MnO2 | B.WO3 | C.Co3O4 | D.CrO3 |
C
根据得失电子守恒有如下关系:
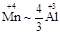
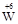 ~2
~2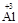
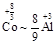
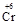 ~2
~2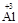 ,所以C消耗铝最少。
,所以C消耗铝最少。
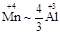
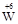 ~2
~2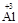
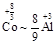
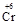 ~2
~2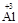 ,所以C消耗铝最少。
,所以C消耗铝最少。
练习册系列答案
相关题目
题目内容
| A.MnO2 | B.WO3 | C.Co3O4 | D.CrO3 |
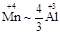
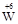 ~2
~2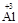
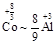
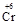 ~2
~2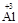 ,所以C消耗铝最少。
,所以C消耗铝最少。