题目内容
11.化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
已知:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$ RCH=CHCOOR’请回答:
(1)A中官能团的名称是羟基;C→D的反应类型为取代反应(或水解反应).
(2)B+D→F的化学方程式
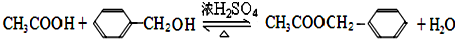 .
.(3)E的结构简式
 .
.(4)对于化合物X,下列说法正确的是AD.
A.能发生水解反应 B.能发生银镜反应
C.不与浓硝酸发生取代反应 D.能使Br2的CCl4溶液褪色
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有5个,请写出不含甲基的一种同分异构体的结构简式
 .
.
分析 乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,则C为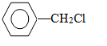 ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为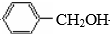 ,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为
,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为 ,据此推断得出F为:
,据此推断得出F为: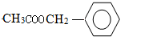 ,那么X为
,那么X为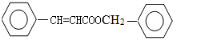 ,据此分析回答即可.
,据此分析回答即可.
解答 解:乙烯与水在催化剂作用下发生加成反应生成乙醇,故A是乙醇,乙醇催化氧化最终生成乙酸,故B是乙酸;甲苯在光照条件下与氯气发生的是取代反应,则C为 ,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为
,C在氢氧化钠的水溶液中发生的是取代反应,那么D应为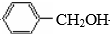 ,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为
,由D能被氧化为E,且结合给出的信息:RCHO+CH3COOR′$\stackrel{CH_{3}CH_{2}ONa}{→}$RCH=CHCOOR′,那么应E为 ,据此推断得出F为:
,据此推断得出F为: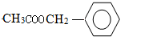 ,那么X为
,那么X为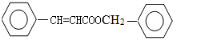 ,
,
(1)A是乙醇,A中官能团的名称是羟基;C→D的反应类型为取代反应,
故答案为:羟基;取代反应;
(2)B为乙酸,D为苯甲醇,两者发生酯化反应生成乙酸苯甲酯,化学反应方程式为: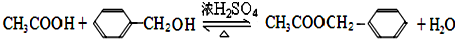 ,
,
故答案为: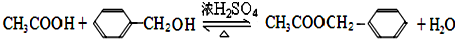 ;
;
(3)根据上面的分析可知,E为 ,
,
故答案为: ;
;
(4)A.X中含有酯基,能发生水解反应,故A正确;
B.X中不含有醛基,不能发生银镜反应,故B错误;
C.X中含有苯环,能与浓硝酸发生取代反应,故C错误;
D.X中含有碳碳双键,能使Br2/CCl4溶液褪色,故D正确,
故答案为:AD;
(5)F有多种同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中四个的结构简式是: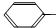 CH2CH2OOCH、
CH2CH2OOCH、 COOCH2CH3、
COOCH2CH3、 CH2COOCH3、
CH2COOCH3、 00CCH2CH3、
00CCH2CH3、 CH(CH3)OOCH,
CH(CH3)OOCH,
故答案为:5; .
.
点评 本题主要考查的是有机物的合成与有机物的推断,充分掌握常见有机化合物的性质以及抓住所给信息解题是关键,难度中等,注意有机官能团的性质的灵活运用.

| A. | 金属的活泼顺序为:a>c>b>d | |
| B. | 在①的溶液中,SO42-向b极移动 | |
| C. | 在③的装置中,一段时间后b电极质量将会减轻 | |
| D. | 二次电池放电时的反应和充电时的反应是可逆反应 |
| 选项 | 物质 | 杂质 | 试剂及操作 |
| A | 氢氧化钠 | 硫酸钠 | 加入适量氢氧化钙,过滤 |
| B | 生石灰 | 碳酸钙 | 高温锻烧 |
| C | 二氧化碳 | 一氧化碳 | 通过有足量灼烧氧化铁的玻璃管 |
| D | 氧化铜粉末 | 木炭粉 | 隔绝空气加强热 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 第三列为ⅠB | B. | 第十三列为ⅢA | C. | 第十六列为ⅣA | D. | 第十八列为0A |
| A. | 油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 | |
| B. | 人的皮肤在强紫外线的照射下将会失去生理活性 | |
| C. | 棉花和蚕丝的主要成分都是纤维素 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
| A. | 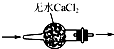 干燥SO2气体 | |
| B. |  蒸发CH3COONa溶液得醋酸钠晶体 | |
| C. |  分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 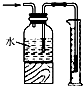 测量氯气的体积 |