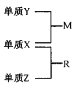
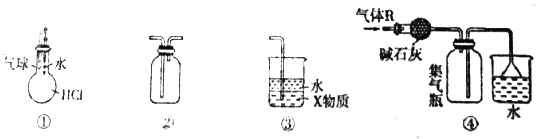
题目内容
【题目】煤燃烧产生的烟气含有的SO2,是大气主要污染物之一。减少煤燃烧对大气造成的污染,应从多方面采取措施。
(1)在煤燃烧前需对煤进行脱硫处理。
①一种烟气脱硫技术是向煤中加入适量石灰石,可大大减少燃烧产物中SO2的含量,最后生成CaSO4,该反应的化学方程式为_________________________________________。
②煤炭中以FeS2(铁元素为+2价)形式存在的硫,可以采用微生物脱硫技术脱去,其原理如图所示:
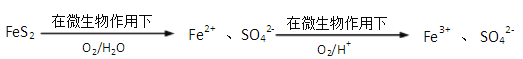
1mol FeS2完全转化为Fe3+ 和SO42-时,FeS2与O2物质的量之比为_____________。
(2)燃煤后烟气脱硫方法之一是利用天然海水的碱性吸收烟气中SO2并转化为无害的SO42-,其流程的示意图如下:
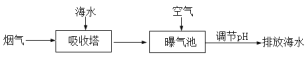
①海水中碳元素主要以HCO3-的形式存在。用离子方程式表示海水呈碱性的原因:_____________。
②研究表明,进入吸收塔的海水温度越低,SO2的脱除效果越好,主要原因是_____________。
③从吸收塔排出的海水呈酸性,并含有较多的HSO3-,排入曝气池进行处理时,需要鼓入大量空气。空气的作用是____________________________________。
【答案】2CaCO3+2SO2 +O2![]() 2CaSO4 +2CO24: 15HCO3- + H2O
2CaSO4 +2CO24: 15HCO3- + H2O ![]() H2CO3 + OH-海水温度越低,SO2在其中的溶解度越大(其他答案合理给分)将HSO3-氧化为SO42-
H2CO3 + OH-海水温度越低,SO2在其中的溶解度越大(其他答案合理给分)将HSO3-氧化为SO42-
【解析】
(1)①向煤中加入石灰石起固硫的作用,该反应的化学方程式是:2CaCO3+2SO2 +O2![]() 2CaSO4 +2CO2;
2CaSO4 +2CO2;
②1mol FeS2完全转化为Fe3+ 和SO42-时,铁元素由+2价变为+3价,硫元素由-1价变为+6价,氧元素由0价变为-2价,故FeS2与O2的计量数为4和15,故物质的量之比为4: 15;
(2)①海水中碳元素主要以HCO3-的形式存在。HCO3-水解使溶液呈碱性,故海水呈碱性的原因为:HCO3- + H2O ![]() H2CO3 + OH-;
H2CO3 + OH-;
②海水温度越低,SO2在其中的溶解度越大,故进入吸收塔的海水温度越低,SO2的脱除效果越好;
③从吸收塔排出的海水呈酸性,并含有较多的HSO3-,排入曝气池进行处理时,需要鼓入大量空气,将HSO3-氧化为SO42-。

【题目】某实验小组研究溶液中AgNO3和Na2S的反应。
实验 | 试剂 | 现象 | |
| 试管 | 滴管 | |
(pH = 4) |
(pH = 9) | 出现黑色沉淀 | |
(1)用离子方程式解释Na2S溶液pH > 7的原因:________。
(2)实验小组同学认为黑色沉淀中可能含有Ag2O、Ag2S或Ag,设计实验验证。
已知:i.浓硝酸能将Ag2S转化为![]() 和
和![]() ;
;
ii.Ag2O能溶解在浓氨水中形成银氨溶液,而Ag2S和Ag均不能。
① 设计并实施如下实验,证实沉淀中含有Ag2S。

试剂1和试剂2分别是_________、_________。
现象1和现象2分别是_________、_________。
② 设计并实施如下实验,证实沉淀中不含有Ag2O,将实验操作和现象补充完整。
实验操作 | 实验现象 | |
步骤i | 取少量银氨溶液,向其中滴加盐酸 | 出现白色沉淀 |
步骤ii | 取少量洗涤后的黑色沉淀,____________ | ____________ |
③ 经检验,沉淀不含有Ag。

(3)实验小组同学认为AgNO3溶液具有氧化性,在一定条件下能够氧化Na2S,设计实验进行研究(实验装置如右图所示),测得电压为a(![]() )。
)。
对AgNO3溶液中氧化![]() 的物质进行推测:
的物质进行推测:
假设1: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() ;
;
假设2: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() 。
。
利用右图装置继续研究(已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大)。
① 将![]() 的AgNO3溶液替换为_______溶液,记录电压为b(
的AgNO3溶液替换为_______溶液,记录电压为b(![]() )。
)。
② 上述实验证实了氧化![]() 的物质中一定包含
的物质中一定包含![]() ,其证据是______。
,其证据是______。
实验结论:AgNO3溶液与Na2S溶液的反应类型与反应条件有关。