题目内容
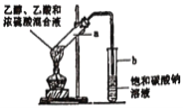
【题目】下图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是

A. 逐滴加入饱和食盐水可控制生成乙炔的速率
B. 用溴水验证乙炔的性质,不需要除杂
C. KMnO4酸性溶液褪色,说明乙炔具有还原性
D. 将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高
【答案】B
【解析】A、电石跟水反应比较剧烈,若向电石中滴加饱和食盐水,电石与水反应,消耗水,使得NaCl在电石表面析出,减少了电石与水的接触,减缓了反应速率,故A正确;B、乙炔气体中混有的硫化氢可以被Br2氧化,对乙炔性质的检验产生干扰,所以应用硫酸铜溶液洗气,故B错误;B、酸性KMnO4溶液具有强氧化性,乙炔使酸性KMnO4溶液褪色,表现了乙炔的还原性,故C正确;D、对于烃类物质而言,不饱和程度越高,则含碳量越高,火焰越明亮,烟越浓,乙炔含有碳碳三键,是不饱和程度较高的烃类物质,故D正确。故选B。

【题目】在2 L密闭容器内,t℃时发生反应:N2(g)+3H2(g)![]() 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为_______________________;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=_____________;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH3)=0.05 mol·L-1·min-1 b.v(H2)=0.03 mol·L-1·min-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.00 l mol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是_____________。
a.反应速率v(N2):v(H2):v(NH3)=1:3:2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2
f.v(N2)消耗=2v(NH3)消耗
g.单位时间内3mol H—H键断裂的同时2mol N—H键也断裂