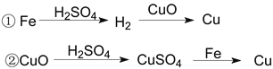题目内容
【题目】H2C2O4为二元弱酸。25 ℃时,向0.100 mol·L1 Na2C2O4溶液中缓缓通入HCl气体(忽略溶液体积的变化)。下列指定溶液中微粒的物质的量浓度关系正确的是
A.0.100 mol·L1 Na2C2O4溶液中:c(C2O42)>c(HC2O4)>c(OH)>c(H+)
B.pH=7的溶液中:c(Cl-)=c(HC2O4)+2c(H2C2O4)
C.c(Cl-)=0.100 mol·L1溶液中:c(OH)c(H+)=c(H2C2O4)c(C2O42)
D.c(HC2O4)=c(C2O42)的酸性溶液中:c(Cl-)+c(HC2O4)<0.100 mol·L1+c(H2C2O4)
【答案】BC
【解析】
A. Na2C2O4分步水解,且一步比一步难,![]() +H2O
+H2O![]()
![]() +OH-,
+OH-,![]() + H2O
+ H2O![]()
![]() +OH-,水也电离出OH-, 故c(OH)>c(HC2O4),故A项错误;
+OH-,水也电离出OH-, 故c(OH)>c(HC2O4),故A项错误;
B. pH=7为中性,c(H+)= c(OH),依据电荷守恒![]() ,再依据物料守恒
,再依据物料守恒![]() ,二者相减即可得到B项关系式,B项正确;
,二者相减即可得到B项关系式,B项正确;
C.当![]() 浓度为0.100mol/L时,可以发现此时有物料守恒
浓度为0.100mol/L时,可以发现此时有物料守恒![]() ,依据电荷守恒有:
,依据电荷守恒有:![]() ,此时溶液中有
,此时溶液中有![]() ,代入后化简得到,c(OH)c(H+)=c(H2C2O4)c(C2O42),C项正确;
,代入后化简得到,c(OH)c(H+)=c(H2C2O4)c(C2O42),C项正确;
D.首先将物料守恒![]() 代入关系式,化简得到
代入关系式,化简得到![]() ,因为溶液是酸性的,结合选项B的分析,应有
,因为溶液是酸性的,结合选项B的分析,应有![]() ,D项错误;
,D项错误;
答案选BC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列根据实验现象得出的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 废FeCl3蚀刻液中加入少量铁粉,振荡 | 得到澄清溶液 | 蚀刻液中一定不含Cu2+ |
B | 将Fe(NO3)2样品溶于H2SO4,滴加KSCN溶液 | 溶液变红 | 稀硫酸能氧化Fe2+ |
C | 向两份蛋白质溶液中分别滴加饱和硫酸钠溶液和硫酸铜溶液 | 均有固体析出 | 蛋白质均发生变性 |
D | 葡萄糖溶液与新制Cu(OH)2混合加热 | 生成砖红色沉淀 | 葡萄糖分子中含有醛基 |
A.AB.BC.CD.D
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
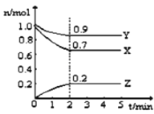
(1)由图中所给数据进行分析,该反应的化学方程式为__________。
(2)若上述反应中X、Y、Z分别为H2、N2 、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
0~50s内的平均反应速率 v(N2) = __________,250s时,H2的转化率为____________。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ/mol。![]() 的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中___(填“吸收”或“放出”)的能量为____, 反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,则生成1molNH3过程中___(填“吸收”或“放出”)的能量为____, 反应达到(2)中的平衡状态时,对应的能量变化的数值为____kJ。
(4)反应达平衡时容器内混合气体的平均相对分子质量比起始时____(填增大、减小或不变),混合气体密度比起始时______(填增大、减小或不变)。
(5)为加快反应速率,可以采取的措施是_______
a.降低温度 b.增大压强 c.恒容时充入He气
d.恒压时充入He气 e.及时分离NH3
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
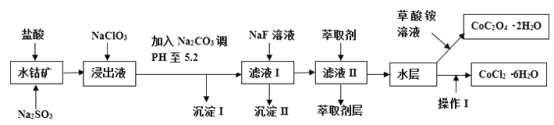
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有两种沉淀;③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子反应方程式为_________________。
(2)NaClO3在浸出液中发生的离子反应方程式为______________。
(3)加入Na2CO3调PH至5.2,目的是________;萃取剂层含锰元素,则沉淀II的主要成分为_____。
(4)操作I包括:将水层加入浓盐酸调整PH为2-3,______、_____、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是_____(回答一条原因即可)。