��Ŀ����
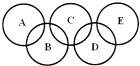
����Ŀ����ҵ���ô��Σ���Ca2+��Mg2+��SO42�������ʣ�Ϊ��Ҫԭ�ϲ��á������Ƽ����������ͻ���NH4Cl��������������ͼ��ʾ�������й�˵����ȷ���� �� �� 
A.�Դ�����Һ���ӿ����μ���NaOH��Na2CO3��BaCl2 �� �ټ������������ҺpH
B.����ʳ��ˮ����ͨ�������ΪCO2
C.����ͼ�е�ϵ�в�����һ����Ҫ������
D.
��ͼ��ʾװ�ÿ��ԱȽ�Na2CO3��NaHCO3��������ȶ���
���𰸡�C
���������⣺A����ȥ�����е�Ca2+��Mg2+��SO42������ɳ�����Լӹ������Ȼ�����ȥ��������ӣ�Ȼ����̼����ȥ�������Ӻ����ı����ӣ�����Ҫ�����������ȥ�������������ƺ�̼���ƣ���A����
B��������̼��ˮ���ܽ�Ƚ�С�������ܽ�Ƚϴ�Ӧ��ͨ�백����������Һ����ͨ�������̼��������̼���ܽ�������Դﵽʵ��Ŀ�ģ���B����
C������Һ�еõ����壬��Ҫ����Ũ������ȴ�ᾧ�����˵Ȳ�������Щ��������Ҫ���������衢�����ȣ���C��ȷ��
D��Na2CO3���Ȳ��ֽ⣬NaHCO3����������ֽ⣬��С�Թ���ʢ��NaHCO3 �� ���Թ���ʢ��Na2CO3 �� NaHCO3��Ӽ����ֽܷ⣬Na2CO3ֱ�Ӽ��Ȳ��ֽ⣬��֤�����ߵ��ȶ��ԣ�ͼ�зŷ�����D����ѡC��

 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�����Ŀ�����и��������в��ܰ���ͼ��ʾ�Ĺ�ϵһ��ת�����ǣ� �� 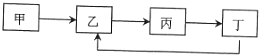
ѡ�� | �� | �� | �� | �� |
A | S | SO2 | SO3 | H2SO4 |
B | Al | Al2O3 | AlCI3 | Al��OH��3 |
C | Na | Na2O2 | Na2CO3 | NaOH |
D | Si | SiO2 | Na2SO3 | H2SiO3 |
A.A
B.B
C.C
D.D