题目内容
Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式: ,该反应是 反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与 有关。
Ⅱ.某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如右图所示,图中数据分析:
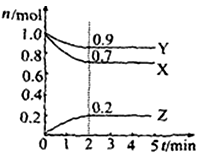
(1)该反应的化学方程式为: 。
(2)反应开始至2min,用Z表示的平均反应速率为: 。
(3)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g) + Y(g) = 2Z(g),当改变下列条件时,反应速率会减小
A.降低温度 B.加入催化剂 C.增大容器体积
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式: ,该反应是 反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与 有关。
Ⅱ.某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如右图所示,图中数据分析:

(1)该反应的化学方程式为: 。
(2)反应开始至2min,用Z表示的平均反应速率为: 。
(3)在密闭容器里,通入a mol X(g)和b mol Y(g),发生反应X(g) + Y(g) = 2Z(g),当改变下列条件时,反应速率会减小
A.降低温度 B.加入催化剂 C.增大容器体积
Ⅰ(1) 2H2O2 2H2O +O2 ↑ ;2分, 放热;1分(2)催化剂接触面积。1分
2H2O +O2 ↑ ;2分, 放热;1分(2)催化剂接触面积。1分
Ⅱ(1)3X + Y 2Z 2分,(2)0.05 mol·L-1·min-1 2分
2Z 2分,(2)0.05 mol·L-1·min-1 2分
(3)AC 2分,少选得1分,错选不得分
 2H2O +O2 ↑ ;2分, 放热;1分(2)催化剂接触面积。1分
2H2O +O2 ↑ ;2分, 放热;1分(2)催化剂接触面积。1分Ⅱ(1)3X + Y
 2Z 2分,(2)0.05 mol·L-1·min-1 2分
2Z 2分,(2)0.05 mol·L-1·min-1 2分(3)AC 2分,少选得1分,错选不得分
试题分析:Ⅰ(1)H2O2在二氧化锰作用下发生反应的化学反应方程式为2H2O2
 2H2O +O2↑,根据试管很烫可知该反应是放热反应。
2H2O +O2↑,根据试管很烫可知该反应是放热反应。(2)根据表中给出的数据可知,在其他条件相同时,粉末状二氧化锰比块状二氧化锰反应所需时间短,说明接触面积对反应速率有影响。
Ⅱ(1)由由图象可以看出,X、Y的物质的量逐渐减小,则X、Y为反应物,Z的物质的量逐渐增多,作为Z为生成物,当反应到达2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,化学反应中,各物质的物质的量的变化值与化学计量数呈正比,则△n(X):△n(Y):△n(Z)=3:1:2,所以反应的化学方程式为:3X + Y
 2Z。
2Z。(2)物质Z浓度的变化量为0.2mol÷2L=0.1mol/L,所以Z物质表示的反应速率为01mol/L÷2min=0.05mol/(L·min)。
(3)A、温度较低反应速率一定是减小的,A正确;B、加入催化剂反应速率可以加快,也可能减小,B不正确;C、增大容器容积,物质的浓度减小,则反应速率减小,C正确,答案选AC。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
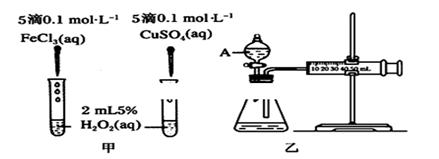
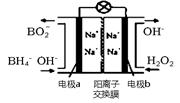
 CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.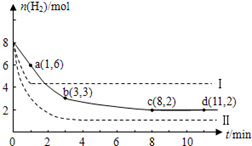
 2NH3(g),△H=-92.4 kJ.mol-1下列叙
2NH3(g),△H=-92.4 kJ.mol-1下列叙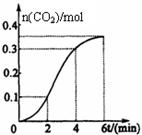
 2NH3。下列关于该反应的说法正确的是
2NH3。下列关于该反应的说法正确的是 2SO3(g) △H=-196 kJ?mol-1。在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3为0.18 mol,则v(O2)= mol?L-1?min-1,放出的热量为 kJ。
2SO3(g) △H=-196 kJ?mol-1。在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3为0.18 mol,则v(O2)= mol?L-1?min-1,放出的热量为 kJ。 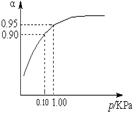
 2NH3,某段时间内的平均反应速率分别用v(N2)、v(H2)、v(NH3)表示(单位均为mol·L-1·s-1)时,下列关系式中正确的是( )
2NH3,某段时间内的平均反应速率分别用v(N2)、v(H2)、v(NH3)表示(单位均为mol·L-1·s-1)时,下列关系式中正确的是( )