题目内容
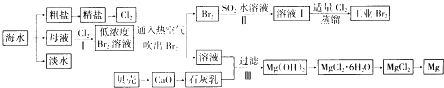
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出),请回答下列问题: 
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 , 反应④的化学方程式为 .
(2)若A是常见的变价金属的单质,D、F是气态单质,反应④可以在光照条件下发生.反应①和反应②在水溶液中进行,反应②的离子方程式是
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 . 标准状况下3.36L物质E与含氢氧化钠10.0g的溶液充分反应,所得溶液中溶质成分为(写出化学式和对应的物质的量).
【答案】
(1) ;C+4HNO3(浓)
;C+4HNO3(浓) ![]() CO2+4NO2↑+2H2O
CO2+4NO2↑+2H2O
(2)Cl2+2Fe2+=2Cl﹣+2Fe3+
(3)2C+SiO2 ![]() Si+2CO↑;Na2CO2 , 0.1mol;NaHCO3 , 0.05mol
Si+2CO↑;Na2CO2 , 0.1mol;NaHCO3 , 0.05mol
【解析】解:(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,则A原子序数是偶数,所含元素的原子最外层电子数D是A的2倍,则A是Mg、D是C元素,F的浓溶液与A、D反应都有红棕色气体生成,红棕色气体是NO2 , 则F是HNO3 , C和HNO3浓溶液反应生成CO2、NO2和H2O,B能和Mg反应生成碳单质,则B是CO2 , C是MgO,MgO和硝酸反应生成Mg(NO3)2和H2O,Mg和硝酸反应生成Mg(NO3)2 , 则E是Mg(NO3)2 , A是Mg,A的原子结构示意图为 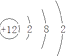 ,反应④的化学方程式为在加热条件下,碳和浓硝酸发生氧化还原反应生成二氧化碳、二氧化氮和水,反应方程式为:C+4HNO3(浓)
,反应④的化学方程式为在加热条件下,碳和浓硝酸发生氧化还原反应生成二氧化碳、二氧化氮和水,反应方程式为:C+4HNO3(浓) ![]() CO2+4NO2↑+2H2O,
CO2+4NO2↑+2H2O,
所以答案是: 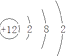 ;C+4HNO3(浓)
;C+4HNO3(浓) ![]() CO2+4NO2↑+2H2O;(2)若A是常见的变价金属的单质,则A是Fe,D、F是气态单质,反应①在水溶液中进行.反应②也在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2 , 氯化亚铁被氯气氧化生成氯化铁,离子反应方程式为:Cl2+2Fe2+=2Cl﹣+2Fe3+ ,
CO2+4NO2↑+2H2O;(2)若A是常见的变价金属的单质,则A是Fe,D、F是气态单质,反应①在水溶液中进行.反应②也在水溶液中进行,则B是酸,C是盐,D和F反应生成酸,盐和气体单质F反应生成E,Fe和气体单质直接反应生成E,则F是Cl2、E是FeCl3、C是FeCl2、B是HCl、D是H2 , 氯化亚铁被氯气氧化生成氯化铁,离子反应方程式为:Cl2+2Fe2+=2Cl﹣+2Fe3+ ,
所以答案是:Cl2+2Fe2+=2Cl﹣+2Fe3+;(3)A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,则B为SiO2 , A、F所含元素同周期,则A为C,D为Si,F为O2 , 根据转化关系,C为CO,E为CO2 , 反应①为C与二氧化硅的反应,该反应为2C+SiO2 ![]() Si+2CO↑,
Si+2CO↑,
将标准状况下3.36L二氧化碳为 ![]() =0.15mol,10.0g 氢氧化钠为
=0.15mol,10.0g 氢氧化钠为 ![]() =0.25mol,二者物质的量之比为3:5,介于2:1与1:1之间,则生成Na2CO3、NaHCO3 , 设二者物质的量分别为xmol、ymol,则
=0.25mol,二者物质的量之比为3:5,介于2:1与1:1之间,则生成Na2CO3、NaHCO3 , 设二者物质的量分别为xmol、ymol,则 ![]() ,解得x=0.1,y=0.05,
,解得x=0.1,y=0.05,
所以答案是:2C+SiO2 ![]() Si+2CO↑;Na2CO2 , 0.1mol;NaHCO3 , 0.05mol.
Si+2CO↑;Na2CO2 , 0.1mol;NaHCO3 , 0.05mol.

 备战中考寒假系列答案
备战中考寒假系列答案