题目内容
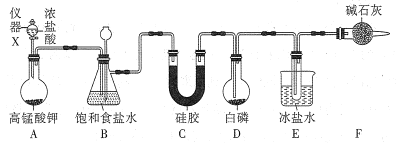
【题目】三氯化磷(PCl3)是一种基础化工原料使用广泛需求量大。实验室可用白磷与氯气反应制备三氯化磷,实验装置如图所示(夹持装置未画出)。
已知:①氯气与白磷反应放出热量(温度高于75℃)。
②PCl3和PCl5遇水强烈反应并产生大量的白雾。
③PCl3和PCl5的物理常数如下:
熔点 | 沸点 | |
PCl3 | -112℃ | 76℃ |
PCl5 | 146℃ | 200℃分解 |
回答下列问题:
(1)仪器X的名称是___;装置A中发生反应的离子方程式为___。
(2)装置B可用于除杂,也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若装置C或D中发生堵塞时B中的现象是__。
(3)为防止装置D因局部过热而炸裂,实验开始前应在圆底烧瓶的底部放少量__(填“干沙”或“水”)。
(4)装置E的烧杯中冰盐水的作用是___。
(5)装置F的作用:一是防止空气中水蒸气的进入;二是___。
(6)前期白磷过量生成PCl3,后期氯气过量生成PCl5,从PC13和PCl5的混合物中分离出PCl3的最佳方法是___。
【答案】分液漏斗 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O 吸滤瓶中液面下降,长颈漏斗中液面上升 干沙 使三氯化磷蒸汽充分冷凝 吸收过量的氯气 蒸馏
【解析】
实验室可用白磷与氯气反应制备三氯化磷:装置A由高锰酸钾与浓盐酸制备氯气,离子反应为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O,制得的氯气混有HCl气体,B装置中的饱和食盐水吸收HCl气体,同时也是安全瓶,能监测实验进行时装置C或D中是否发生堵塞,若发生堵塞,吸滤瓶中液面下降,长颈漏斗中液面上升,C装置干燥氯气,纯净干燥的氯气在D中与白磷反应生成三氯化磷,E装置冷凝三氯化磷蒸汽,装置F防止空气中水蒸气的进入,同时吸收过量的氯气,防止污染空气。
(1)根据图示仪器X为分液漏斗;装置A中由高锰酸钾与浓盐酸制备氯气,反应为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;故答案为:分液漏斗;2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;
(2)装置C或D中是否发生堵塞,则装置B中气体压强增大,会把吸滤瓶中的液体压入长颈漏斗中,导致吸滤瓶中液面下降,长颈漏斗中液面上升;故答案为:吸滤瓶中液面下降,长颈漏斗中液面上升;
(3)为防止装置D因局部过热而炸裂,通常会在底部铺上一层沙子或加入一定量的水,因为三氯化磷会水解,所以只能用干沙;故答案为:干沙;
(4)三氯化磷熔沸点低,通过降温可将其转化为液体,在E中收集;故答案为:使三氯化磷蒸汽充分冷凝;
(5)氯气是有毒气体,未反应完的氯气会造成大气污染,空气中的水蒸气进入D装置也会影响三氯化磷的制备。所以装置F的作用:一是防止空气中水蒸气的进入E,引起三氯化磷的水解,二是吸收过量的氯气,防止污染空气;故答案为:吸收过量的氯气;
(6)氯气逐渐过量会将PCl3氧化生成PCl5,根据表,随PCl3是液态,PCl5是固态,但在加热时温度都超过75℃,此时PCl3是气态,PCl5是液态,可以蒸馏分开;故答案为:蒸馏。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极![]() 接通电源,经过一段时间后,乙中c电极质量增加
接通电源,经过一段时间后,乙中c电极质量增加![]() 据此回答问题:
据此回答问题:
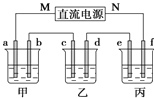
(1)电源的M端为_____________极;
(2)电极d上发生的电极反应式为__________; 乙池溶液PH__________填(“增大”、“减小”或“不变”)
(3)甲池中的总反应式为___________________________________;
(4)当电路中有0.04mol电子通过时,a、b、c、d电极上产生的气体或固体的物质的量之比是____________;
(5)若利用丙池实现铁上镀铜,则“e-f-x”![]() 溶液是__________________________;(要求e、f、x用具体物质回答,下同),若利用丙池实现电解精炼铜,则f电极材料是_______________________
溶液是__________________________;(要求e、f、x用具体物质回答,下同),若利用丙池实现电解精炼铜,则f电极材料是_______________________
(6) 实验测得, 1g甲醇(CH3OH)液体在氧气中充分燃烧生成二氧化碳气体和液态水时释放出22.68kJ的热量,则表示甲醇燃烧热的热化学方程式为:_____________________________________________________
(7)亚硝酸氯![]() 结构式为
结构式为![]() 是有机合成中的重要试剂,可由
是有机合成中的重要试剂,可由![]() 和
和![]() 在通常反应条件下制得,反应方程式为
在通常反应条件下制得,反应方程式为![]() 。已知几种化学键的键能数据如下表所示:
。已知几种化学键的键能数据如下表所示:
化学键 |
|
|
|
|
键能 | 243 | a | 607 | 630 |
当![]() 与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为______kJ。(用数字和字母表示)
与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为______kJ。(用数字和字母表示)