题目内容
【题目】氧化剂和还原剂在生产生活中广泛使用.已知高锰酸钾和浓盐酸可以发生如下反应:
2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
(1)在该反应中还原剂为 , 还原产物为
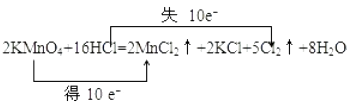
(2)用双线桥表示该反应中电子转移的方向和数目2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
(3)若有0.8mol还原剂被氧化,则转移电子的物质的量是 .
【答案】
(1)HCl;MnCl2
(2)
(3)0.8 mol
【解析】解:(1.)反应2KMnO4+16HCl=2MnCl2↑+2KCl+5C12↑+8H2O,KMnO4中Mn化合价由+7降低到+2,则KMnO4为氧化剂,生成MnCl2为还原产物,
16HCl中有10HCl的Cl化合价由﹣1升高到0价,所以还原剂为HCl,所以答案是:HCl;MnCl2;
(2.)反应2KMnO4+16HCl=2MnCl2↑+2KCl+5C12↑+8H2O,KMnO4中Mn化合价由+7降低到+2,则KMnO4为氧化剂,生成MnCl2为还原产物,
16HCl中有10HCl的Cl化合价由﹣1升高到0价,转移电子数为10mol,所以双线桥表示为:  ,
,
所以答案是:  ;
;
(3.)反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,还原剂HCl的Cl化合价由﹣1升高到0价,所以有0.8mol还原剂被氧化,则转移电子的物质的量是0.8 mol,所以答案是:0.8 mol.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目