��Ŀ����
����Ŀ��X��Y��Z��W��R�Ƕ�����Ԫ�أ�ԭ�������������ǽ���Xԭ�Ӻ�����������֮��Ϊ1��2��Yԭ�Ӻ�Zԭ�ӵĺ��������֮��Ϊ20��W��R��ͬ��������Ԫ�أ�Y���������R������������γ����꣮��ش��������⣺
��1��Ԫ��X�����������ĵ���ʽΪ��Ԫ��Z�����ӽṹʾ��ͼΪ ��
��2������ͭ��Ԫ��Y������������Ӧˮ�����ϡ��Һ������Ӧ�Ļ�ѧ����ʽΪ ��
��3��Ԫ��Wλ�����ڱ��ĵ��壬��ǽ����Ա�R������ԭ�ӽṹ��֪ʶ����ԭ�� ��
��4��R��һ����������ʹƷ����Һ��ɫ����ҵ����Y����̬�⻯���ˮ��Һ��������������ռ���д�����ռ��������������ﷴӦ�����ӷ���ʽ�� ��
��5��Y��Z��ɵĻ�����ZY�������������������Ԫ������ҵ����Z�������X���ʺ�Y�����ڸ������Ʊ�ZY������Z���������X���ʵ����ʵ���֮��Ϊ1��3����÷�Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1��![]() ��
��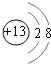
��2��8HNO3��ϡ��+3Cu�T2NO��+3Cu��NO3��2+4H2O
��3���������ڵ�VA�壻Pԭ�Ӻ�Sԭ�ӵĵ��Ӳ�����ͬ��Pԭ�Ӱ뾶�ϴõ�����������
��4��SO2+NH3?H2O�THSO ![]() +NH
+NH ![]()
��5��Al2O3+3C+N2 ![]() 2AlN+3CO
2AlN+3CO
���������⣺X��Y��Z��W��R�Ƕ�����Ԫ�أ�ԭ��������������Y���������R������������γ����꣬��YΪNԪ�ء�RΪSԪ�أ�W��R��ͬ��������Ԫ�أ���WΪPԪ�أ�Yԭ�Ӻ�Zԭ�ӵĺ��������֮��Ϊ20����Zԭ�Ӻ��������=20��7=13����ZΪAl���ǽ���Xԭ�Ӻ�����������֮��Ϊ1��2��X��2�����Ӳ㣬XΪCԪ�أ���1��Ԫ��X�����������ΪCO2 �� ������Cԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ ![]() ��Ԫ��Z������ΪAl3+ �� ���Ӻ��������Ϊ10�����������Ϊ2��8�����ӽṹʾ��ͼΪ
��Ԫ��Z������ΪAl3+ �� ���Ӻ��������Ϊ10�����������Ϊ2��8�����ӽṹʾ��ͼΪ 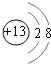 �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
�� 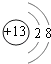 ����2������ͭ��ϡ���ᷴӦ��������ͭ��NO��ˮ����Ӧ����ʽΪ��8HNO3��ϡ��+3Cu�T2NO��+3Cu��NO3��2+4H2O�����Դ��ǣ�8HNO3��ϡ��+3Cu�T2NO��+3Cu��NO3��2+4H2O����3��Ԫ��WΪP��������3�����Ӳ㣬����������Ϊ5��λ�����ڱ��ĵ������ڵ�VA�壻Pԭ�Ӻ�Sԭ�ӵĵ��Ӳ�����ͬ��Pԭ�Ӱ뾶�ϴõ���������������P�ķǽ����Ա�Ԫ��S�������Դ��ǣ��������ڵ�VA�壻Pԭ�Ӻ�Sԭ�ӵĵ��Ӳ�����ͬ��Pԭ�Ӱ뾶�ϴõ���������������4��R��һ����������ʹƷ����Һ��ɫ����������ΪSO2 �� ��ҵ���ð���ˮ��Һ��������������ռ������ռ��������������ﷴӦ�����ӷ���ʽ��SO2+NH3H2O�THSO
����2������ͭ��ϡ���ᷴӦ��������ͭ��NO��ˮ����Ӧ����ʽΪ��8HNO3��ϡ��+3Cu�T2NO��+3Cu��NO3��2+4H2O�����Դ��ǣ�8HNO3��ϡ��+3Cu�T2NO��+3Cu��NO3��2+4H2O����3��Ԫ��WΪP��������3�����Ӳ㣬����������Ϊ5��λ�����ڱ��ĵ������ڵ�VA�壻Pԭ�Ӻ�Sԭ�ӵĵ��Ӳ�����ͬ��Pԭ�Ӱ뾶�ϴõ���������������P�ķǽ����Ա�Ԫ��S�������Դ��ǣ��������ڵ�VA�壻Pԭ�Ӻ�Sԭ�ӵĵ��Ӳ�����ͬ��Pԭ�Ӱ뾶�ϴõ���������������4��R��һ����������ʹƷ����Һ��ɫ����������ΪSO2 �� ��ҵ���ð���ˮ��Һ��������������ռ������ռ��������������ﷴӦ�����ӷ���ʽ��SO2+NH3H2O�THSO ![]() +NH
+NH ![]() �����Դ��ǣ�SO2+NH3H2O�THSO
�����Դ��ǣ�SO2+NH3H2O�THSO ![]() +NH
+NH ![]() ����5��N��Al��ɵĻ�����AlN�������������������Ԫ������ҵ������������̼�������ڸ������Ʊ���������������̼�����ʵ���֮��Ϊ1��3��˵��������CO����÷�Ӧ�Ļ�ѧ����ʽΪ��Al2O3+3C+N2
����5��N��Al��ɵĻ�����AlN�������������������Ԫ������ҵ������������̼�������ڸ������Ʊ���������������̼�����ʵ���֮��Ϊ1��3��˵��������CO����÷�Ӧ�Ļ�ѧ����ʽΪ��Al2O3+3C+N2 ![]() 2AlN+3CO�����Դ��ǣ�Al2O3+3C+N2
2AlN+3CO�����Դ��ǣ�Al2O3+3C+N2 ![]() 2AlN+3CO��
2AlN+3CO��

����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷����ɵ�ص�ͭñ(Zn��Cu�ܺ���ԼΪ99%)����ͭ���Ʊ�ZnO�IJ���ʵ��������£�
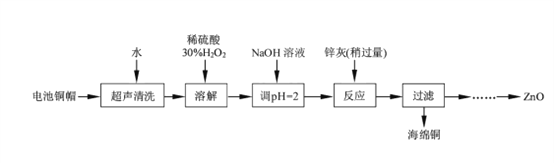
��1����ͭñ�ܽ�ʱ����H2O2��Ŀ����_______________���û�ѧ����ʽ��ʾ����
��ͭñ�ܽ���轫��Һ�й���H2O2��ȥ����ȥH2O2�ļ�㷽����_________________��
��2��Ϊȷ������п������Ҫ�ɷ�ΪZn��ZnO������Ϊ��������������������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㡣���������е����ӷ���ʽ���£�2Cu2����4I��=2CuI(��ɫ)����I2��I2��2S2O32��=2I����S4O62��
�ٵζ�ѡ�õ�ָʾ��Ϊ________________���ζ��յ�۲쵽������Ϊ________________��
�����ζ�ǰ��Һ��H2O2û�г��������ⶨ��Cu2���ĺ�������______________������ƫ������ƫ����������������
��3����֪pH��11ʱZn(OH)2������NaOH��Һ����[Zn(OH)4]2�����±��г��˼����������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol/L������
��ʼ������pH | ��ȫ������pH | |
Fe3�� | 1.1 | 3.2 |
Fe2�� | 5.8 | 8.8 |
Zn2�� | 5.9 | 8.9 |
ʵ���п�ѡ�õ��Լ���30% H2O2��1.0 mol��L��1HNO3��1.0 mol��L��1 NaOH��
�ɳ�ȥͭ����Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��������Һ�м���30%��H2O2ʹ���ַ�Ӧ��
�ڵμ�1.0 moL/L���������ƣ�����pHԼΪ_________________��ʹFe3��������ȫ��
�۹��ˣ�
������Һ�еμ�1.0 moL/L���������ƣ�����pHԼΪ________��ʹZn2��������ȫ��
��____________________________��
��900�����ա�