题目内容
【题目】Cl2和SO2都具有漂白作用,能使品红溶液褪色。若将等物质的量的Cl2、SO2混合后再通入品红与BaCl2的混合溶液,能观察到的现象是( )
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①②B.①③C.②③D.②④
【答案】C
【解析】
等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,发生反应:SO2+Cl2+2H2O=2HCl+H2SO4,生成盐酸和硫酸都不具有漂白性,所以不能使品红溶液;硫酸与氯化钡反应生成硫酸钡沉淀,H2SO4+BaCl2=BaSO4↓+2HCl,所以会产生白色沉淀,②③正确,故答案为C。

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
【题目】下列说法正确的是( ) ①1mol O2的质量是32gmol﹣1;②H2的摩尔质量是2g;③1mol H+的质量是1g;④对原子而言,摩尔质量就是相对原子质量.
A.①②③
B.③④
C.③
D.②④
【题目】工业上用过量的乙酸和异成醇制备乙酸异戊酯,原理(如图所示) 和有关数据如下:
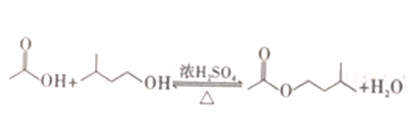
物质 | 相对分子质量 | 密度/(g·cm-3) | 熔点/℃ | 沸点/℃ | 水中溶解度 |
异戊醇 | 88 | 0.8123 | -117 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 17 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | -78 | 142 | 难溶 |
下列说法正确的是
A. 常温下,可用过滤的方法分离乙酸异戊酯和水溶液
B. 反应中,加入过量的乙酸的主要目的是加快该反应的反应速率
C. 为了除去产物中混有的乙酸,可以向混合物中加入足量饱和Na2CO3溶液,充分振荡后静置、分液
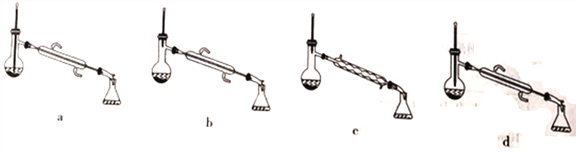
D. 为了除去产物中混有的异戊醇,应选择如图所示装置中的c装置