题目内容
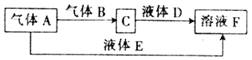
 甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),且存在如下转化关系:甲+乙一丙+丁.依次回答下列问题:
甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),且存在如下转化关系:甲+乙一丙+丁.依次回答下列问题:(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①若丙为可燃性气体,分子的空间构型为直线形结构.写出实验室制备丙的化学方程式
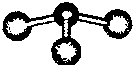
②若甲是由N和Cl元素组成的化合物,其分子球棍模型如图所示,丙具有漂白性.则甲中Cl元素的化合价是
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,写出发生反应的化学方程式
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂.写出甲+乙→+丙+丁的化学方程式
③若甲是由N和0元素组成的气态物质,呈红棕色.将3.36g Fe加到一定量丙溶液中,收集到1.12L气体丁(已折算为标准状况),则反应的离子方程式是
分析:甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),且存在转化关系:甲+乙一丙+丁,
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①若丙为可燃性气体,分子的空间构型为直线形结构,则丙为CH≡CH,甲为CaC2、丁为Ca(OH)2;
②若甲是由N和Cl元素组成的化合物,由甲分子球棍模型可知,较大球为Cl原子、较小球为N原子,甲为NCl3,甲发生水解反应丙具有漂白性,则丙为HClO、丁为NH3,可知NCl3中N表现负价、Cl为正价;
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,则甲为Na2O2,与水反应生成氢氧化钠与氧气;
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂,则丙为CO,故甲为碳、丁为氢气;
③若甲是由N和O元素组成的气态物质,呈红棕色,则甲为NO2,与水反应生成硝酸与NO,Fe加到一定量丙溶液中气体丁,则丙为硝酸、丁为NO,令溶液中Fe3+、Fe2+的物质的量分别为xmol、ymol,根据铁元素守恒、电子守恒数目守恒列方程计算,据此书写.
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①若丙为可燃性气体,分子的空间构型为直线形结构,则丙为CH≡CH,甲为CaC2、丁为Ca(OH)2;
②若甲是由N和Cl元素组成的化合物,由甲分子球棍模型可知,较大球为Cl原子、较小球为N原子,甲为NCl3,甲发生水解反应丙具有漂白性,则丙为HClO、丁为NH3,可知NCl3中N表现负价、Cl为正价;
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,则甲为Na2O2,与水反应生成氢氧化钠与氧气;
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂,则丙为CO,故甲为碳、丁为氢气;
③若甲是由N和O元素组成的气态物质,呈红棕色,则甲为NO2,与水反应生成硝酸与NO,Fe加到一定量丙溶液中气体丁,则丙为硝酸、丁为NO,令溶液中Fe3+、Fe2+的物质的量分别为xmol、ymol,根据铁元素守恒、电子守恒数目守恒列方程计算,据此书写.
解答:解:甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),存在转化关系:甲+乙一丙+丁,
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①若丙为可燃性气体,分子的空间构型为直线形结构,则丙为CH≡CH,甲为CaC2、丁为Ca(OH)2,实验室制备丙的化学方程式为:CaC2+2H2O=Ca(OH)2+HC≡CH↑,
故答案为:CaC2+2H2O=Ca(OH)2+HC≡CH↑;
②若甲是由N和Cl元素组成的化合物,由甲分子球棍模型可知,较大球为Cl原子、较小球为N原子,甲为NCl3,甲发生水解反应丙具有漂白性,则丙为HClO、丁为NH3,故NCl3中N表现负价、Cl为正价,则NCl3中N为-3价、Cl为+1价,
故答案为:+1;
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,则甲为Na2O2,与水反应生成氢氧化钠与氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂,则丙为CO,故甲为碳、丁为氢气,该反应方程式为:C+H2O
CO+H2,
故答案为:C+H2O
CO+H2;
③若甲是由N和O元素组成的气态物质,呈红棕色,则甲为NO2,与水反应生成硝酸与NO,Fe加到一定量丙溶液中气体丁,则丙为硝酸、丁为NO,令溶液中Fe3+、Fe2+的物质的量分别为xmol、ymol,则:
解得x=0.03、y=0.03,
故反应离子方程式为:6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O,
故答案为:6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O.
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
①若丙为可燃性气体,分子的空间构型为直线形结构,则丙为CH≡CH,甲为CaC2、丁为Ca(OH)2,实验室制备丙的化学方程式为:CaC2+2H2O=Ca(OH)2+HC≡CH↑,
故答案为:CaC2+2H2O=Ca(OH)2+HC≡CH↑;
②若甲是由N和Cl元素组成的化合物,由甲分子球棍模型可知,较大球为Cl原子、较小球为N原子,甲为NCl3,甲发生水解反应丙具有漂白性,则丙为HClO、丁为NH3,故NCl3中N表现负价、Cl为正价,则NCl3中N为-3价、Cl为+1价,
故答案为:+1;
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,则甲为Na2O2,与水反应生成氢氧化钠与氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂,则丙为CO,故甲为碳、丁为氢气,该反应方程式为:C+H2O
| ||
故答案为:C+H2O
| ||
③若甲是由N和O元素组成的气态物质,呈红棕色,则甲为NO2,与水反应生成硝酸与NO,Fe加到一定量丙溶液中气体丁,则丙为硝酸、丁为NO,令溶液中Fe3+、Fe2+的物质的量分别为xmol、ymol,则:
|
解得x=0.03、y=0.03,
故反应离子方程式为:6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O,
故答案为:6Fe+5NO3-+2OH-=3Fe3++3Fe2++5NO↑+10H2O.
点评:本题考查无机物的推断、常用化学用语等,难度中等,需要学生熟练掌握元素化合物性质,(2)中注意利用氧化还原反应电子转移守恒计算确定产物.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目