题目内容
甲烷和氨在国民经济中占有重要地位。
(1)制备合成氨原料气H2,可用甲烷蒸汽转化法,主要转化反应如下:
CH4(g) + H2O(g) CO(g) + 3H2(g) ΔH =" +206.2" kJ/mol
CO(g) + 3H2(g) ΔH =" +206.2" kJ/mol
CH4(g) + 2H2O(g) CO2(g) +4H2(g) ΔH = +165.0kJ/mol
CO2(g) +4H2(g) ΔH = +165.0kJ/mol
上述反应所得原料气中的CO能使氨合成催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是 。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g) CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
① 反应热ΔH(填“>”、“<”或“=”)_______0。
② 在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)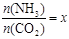 ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。

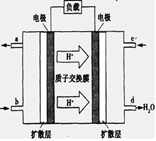
(3)已知甲烷燃料电池的工作原理如下图所示。该电池工作时,a口放出的物质为_________,该电池正极的电极反应式为:____ ,工作一段时间后,当3.2g甲烷完全反应生成CO2时,有 mol 电子发生转移。
(1)制备合成氨原料气H2,可用甲烷蒸汽转化法,主要转化反应如下:
CH4(g) + H2O(g)
 CO(g) + 3H2(g) ΔH =" +206.2" kJ/mol
CO(g) + 3H2(g) ΔH =" +206.2" kJ/molCH4(g) + 2H2O(g)
 CO2(g) +4H2(g) ΔH = +165.0kJ/mol
CO2(g) +4H2(g) ΔH = +165.0kJ/mol上述反应所得原料气中的CO能使氨合成催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是 。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g)
 CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
① 反应热ΔH(填“>”、“<”或“=”)_______0。
② 在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
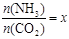 ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。求图中的B点处,NH3的平衡转化率。
(3)已知甲烷燃料电池的工作原理如下图所示。该电池工作时,a口放出的物质为_________,该电池正极的电极反应式为:____ ,工作一段时间后,当3.2g甲烷完全反应生成CO2时,有 mol 电子发生转移。

(16分)
(1)CO(g)+H2O(g) CO2(g)+H2(g) ΔH = -41.2 kJ/mol (3分)
CO2(g)+H2(g) ΔH = -41.2 kJ/mol (3分)
(2)① < (2分)
②32% (计算过程见解析)
(3)CO2(2分) O2+4e-+4H+=2H2O(2分) 1.6 (2分)
(1)CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH = -41.2 kJ/mol (3分)
CO2(g)+H2(g) ΔH = -41.2 kJ/mol (3分)(2)① < (2分)
②32% (计算过程见解析)
(3)CO2(2分) O2+4e-+4H+=2H2O(2分) 1.6 (2分)
试题分析:(1)先对已知热化学方程式编号为①②,观察发现②—①可得,CO(g)+H2O(g)
 CO2(g)+H2(g),其焓变=②的焓变—①的焓变=ΔH = -41.2 kJ/mol,由此可得一氧化碳交换反应的热化学方程式为CO(g)+H2O(g)
CO2(g)+H2(g),其焓变=②的焓变—①的焓变=ΔH = -41.2 kJ/mol,由此可得一氧化碳交换反应的热化学方程式为CO(g)+H2O(g)  CO2(g)+H2(g) ΔH = -41.2 kJ/mol;(2)①读表格中信息可得,随着温度的升高,该反应的平衡常数逐渐减小,根据平衡移动原理和平衡常数计算表达式可知,升高温度平衡向吸热方向移动,平衡常数减小时平衡向逆反应方向移动,因此逆反应是吸热反应,正反应是放热反应,正反应的反应热△H<0;B点的横坐标为4.0,纵坐标为64%,依题意可知n(NH3)/n(CO2)=4.0,CO2的平衡转化率为64%,设起始时CO2的物质的量为1mol,则NH3的物质的量为4.0mol,CO2的变化物质的量为0.64mol,则:
CO2(g)+H2(g) ΔH = -41.2 kJ/mol;(2)①读表格中信息可得,随着温度的升高,该反应的平衡常数逐渐减小,根据平衡移动原理和平衡常数计算表达式可知,升高温度平衡向吸热方向移动,平衡常数减小时平衡向逆反应方向移动,因此逆反应是吸热反应,正反应是放热反应,正反应的反应热△H<0;B点的横坐标为4.0,纵坐标为64%,依题意可知n(NH3)/n(CO2)=4.0,CO2的平衡转化率为64%,设起始时CO2的物质的量为1mol,则NH3的物质的量为4.0mol,CO2的变化物质的量为0.64mol,则:2NH3(g) + CO2(g)
 CO(NH2)2(l) + H2O(l)
CO(NH2)2(l) + H2O(l)起始物质的量(mol) 4.0 1.0
变化物质的量(mol) 1.28 0.64
平衡物质的量(mol) 2.72 0.36
则NH3的平衡转化率:α(NH3)=
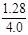 ×100% = 32%
×100% = 32%(3)燃料电池工作时,内电路中氢离子从负极向正极移动,观察甲烷酸性燃料电池装置图可知,左边电极为负极,右边电极为正极,甲烷在负极上发生氧化反应,生成的二氧化碳气体难溶于酸性电解质溶液,则a口放出的物质是二氧化碳气体;氧气在正极上发生还原反应,根据电子、电荷、原子守恒原理可得:O2+4e—+4H+=2H2O (注意不能写成O2+4e—+2H2O=4OH—,因为酸性电解质溶液中不能大量存在氢氧根离子);由于甲烷的相对分子质量为16,则3.2g甲烷的物质的量为0.2mol,负极反应式为CH4—8e—+2H2O=CO2+8H+,其中转移电子与甲烷的系数之比等于物质的量之比,则转移电子的物质的量为1.6mol。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
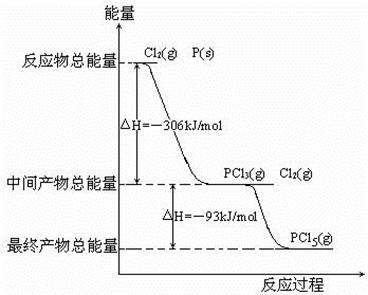
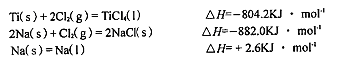
 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H
 HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计)
HSO3—的平衡常数K="8.0" × 106 L?mol-1,计算时SO2、H2SO3的浓度忽略不计) 2NH3(g) △H=-93.0kJ /mol;另据报道,一定条件下:2N2(g)+6H2O(l)
2NH3(g) △H=-93.0kJ /mol;另据报道,一定条件下:2N2(g)+6H2O(l)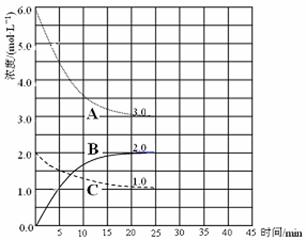
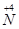 向
向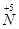 的转化,请你提出一条可行性建议 。
的转化,请你提出一条可行性建议 。 2CO2+N2。
2CO2+N2。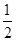 O2(g)=CO2(g) △H=-283.0kJ·mol-1
O2(g)=CO2(g) △H=-283.0kJ·mol-1 C(CO)/mol·L-1
C(CO)/mol·L-1
 2.70×10-3
2.70×10-3