题目内容
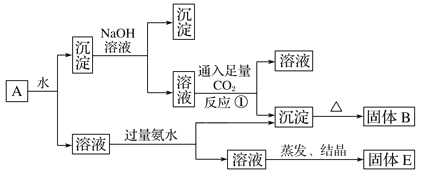
【题目】物质X是某新型净水剂的中间体,它可以看成由氯化铝(在180 ℃升华)和一种盐A按物质的量之比1∶2组成。在密闭容器中加热8.75 g X使之完全分解,冷却后可得到3.2 g固体氧化物B、0.448 L无色气体D(体积已折算为标准状况)、4.27 g混合晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红溶液褪色。请回答下列问题:
(1)X的化学式为_________。
(2)将A固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、D和另一种化合物,则A分解的化学方程式为_____________________________________________________。
(3)将E混合晶体溶于水配成溶液,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为________________________________。
E混合晶体中某种物质在一定条件下能和KI固体反应,写出该方程式:___________________。
(4)高温下,若在密闭容器中长时间煅烧X,产物中还有另外一种气体,其分子式是________。请设计实验方案验证之____________________________________________________________。
【答案】 AlCl3·2FeSO4 2FeSO4![]() SO2↑+SO3+Fe2O3 Al3++2H++6OH-===AlO
SO2↑+SO3+Fe2O3 Al3++2H++6OH-===AlO![]() +4H2O 2KI+SO3
+4H2O 2KI+SO3![]() K2SO3+I2 O2 将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2(其他答案,合理也可)
K2SO3+I2 O2 将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2(其他答案,合理也可)
【解析】固体氧化物B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色,说明B中含有+3价Fe,则B为Fe2O3,无色气体D能使品红溶液褪色,则D为SO2,由元素守恒可知A中含有Fe、S、O元素,A加热分解能生成氧化铁和二氧化硫,则盐A为FeSO4,X的组成为AlCl3·2FeSO4,氧化铁的物质的量为![]() =0.02 mol,生成二氧化硫的物质的量为
=0.02 mol,生成二氧化硫的物质的量为![]() =0.02 mol,由Fe、S原子之比为1∶1,可知生成SO3的物质的量为0.02 mol,4.27 g混合晶体E为AlCl3和SO3,AlCl3的物质的量为
=0.02 mol,由Fe、S原子之比为1∶1,可知生成SO3的物质的量为0.02 mol,4.27 g混合晶体E为AlCl3和SO3,AlCl3的物质的量为![]() =0.02 mol。
=0.02 mol。
(1)X的化学式为AlCl3·2FeSO4。(2)A分解的化学方程式为2FeSO4![]() SO2↑+SO3+Fe2O3。(3)将E混合晶体溶于水配成溶液,三氧化硫与水反应生成硫酸,则硫酸与氯化铝的物质的量相等,逐滴加入过量稀NaOH溶液,该过程总反应的离子方程式为Al3++2H++6OH-===AlO
SO2↑+SO3+Fe2O3。(3)将E混合晶体溶于水配成溶液,三氧化硫与水反应生成硫酸,则硫酸与氯化铝的物质的量相等,逐滴加入过量稀NaOH溶液,该过程总反应的离子方程式为Al3++2H++6OH-===AlO![]() +4H2O;E晶体中的SO3在一定条件下能和KI固体反应,该反应方程式为SO3+2KI===I2+K2SO3。(4)若在高温下长时间煅烧X,生成的三氧化硫再分解生成二氧化硫和氧气,另一种气体分子式是O2,检验氧气的方法:将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2。
+4H2O;E晶体中的SO3在一定条件下能和KI固体反应,该反应方程式为SO3+2KI===I2+K2SO3。(4)若在高温下长时间煅烧X,生成的三氧化硫再分解生成二氧化硫和氧气,另一种气体分子式是O2,检验氧气的方法:将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案