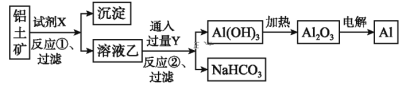
题目内容
【题目】(1)钠在自然界中只能以___________态存在,金属钠通常保存在____________里,它与水反应的化学方程式为:______________________________________________________。
(2)铝与氢氧化钠溶液反应的离子方程式为________________________________,实验室制备氢氧化铝常采用铝盐与氨水反应,写出氯化铝与氨水反应的离子方程式:_________________________。
(3)铁与水蒸气反应的化学方程式为:_____________________________。
(4)简述检验Fe3+的实验操作:___________________________________。
【答案】化合态 煤油 2Na+2H2O= 2NaOH+H2↑ 2Al+2OH+2H2O=2NaAlO2+3H2↑ Al3++3NH3H2O=Al(OH)3↓+3NH4+ 3Fe+4H2O(g)![]() Fe3O4+4H2 取少量滤液于试管中,滴入几滴KSCN溶液,若溶液变血红色,证明含有铁离子,否则无铁离子
Fe3O4+4H2 取少量滤液于试管中,滴入几滴KSCN溶液,若溶液变血红色,证明含有铁离子,否则无铁离子
【解析】
(1)钠是很活泼的金属,在无条件下就能与氧气反应,所以在自然界中只能以化合态存在;钠的密度小于煤油的密度,且和煤油不反应,所以金属钠通常保存在煤油里;钠与水反应生成氢氧化钠和氢气;
(2)铝单质与氢氧化钠溶液反应生成偏铝酸钠和氢气,AlCl3与氨水反应生成氢氧化铝沉淀,一水合氨为弱电解质,保留化学式;
(3)在高温下,铁粉和水蒸气反应,产物有四氧化三铁和氢气;
(4)检验滤液中是否含有Fe3+的简单方法是滴入几滴KSCN溶液,观察溶液是否变红色;
(1)钠是很活泼的金属,在无条件下就能与氧气反应,所以在自然界中只能以化合态存在;钠的密度小于煤油的密度,且和煤油不反应,所以金属钠通常保存在煤油里;2Na+2H2O= 2NaOH+H2↑,
故答案为:化合态;煤油;2Na+2H2O= 2NaOH+H2↑;
(2)铝单质与氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH+2H2O=2NaAlO2+3H2↑;AlCl3与氨水反应的离子方程式为:Al3++3NH3.H2O=Al(OH)3↓+3NH4+,
故答案为:2Al+2OH+2H2O=2NaAlO2+3H2↑;Al3++3NH3H2O=Al(OH)3↓+3NH4+;
(3)在高温下,铁粉和水蒸气反应,产物有四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g)![]() Fe3O4+4H2,
Fe3O4+4H2,
故答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(4)检验是否含有Fe3+的简单方法是滴入几滴KSCN溶液,观察溶液是否变红色,若溶液变红色证明含有Fe3+,否则不含;
故答案为:取少量滤液于试管中,滴入几滴KSCN溶液,若溶液变血红色,证明含有铁离子,否则无铁离子。

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案