题目内容
【题目】600℃时,在 2 L 的恒容密闭容器中充入一定量的 CO 和 H2O,发生反应: CO (g)+H2O (g) ![]() CO2(g)+H2 (g)。反应过程中的部分数据如下表所示:
CO2(g)+H2 (g)。反应过程中的部分数据如下表所示:
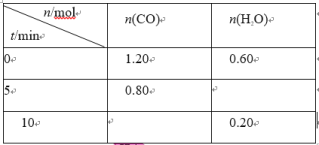
下列说法正确的是
A.0~5 min 用 CO 表示的平均反应速率为 0.08mol·L1·min1
B.该反应在 10 min 后才达到平衡
C.温度升高至 800℃时,反应平衡常数为 0.64,则正反应为吸热反应
D.保持其他条件不变,起始时向容器中充入 0.60 molCO 和 1.20 molH2O,达到平衡时 n(CO2)=0.4mol
【答案】D
【解析】
5 min时,CO减少1.20mol-0.80mol=0.40mol,H2O也减少0.40mol,0.60mol-0.40mol=0.20mol,说明5min时已经达到平衡。
A.0~5 min 用 CO 表示的平均反应速率为![]() =0.04mol·L1·min1,故A错误;
=0.04mol·L1·min1,故A错误;
B.该反应在 5 min 时已经达到平衡,故B错误;
C.600℃时,原平衡常数为![]() =1,温度升高至 800℃时,反应平衡常数为 0.64,升高温度,平衡逆向移动,则正反应为放热反应,故C错误;
=1,温度升高至 800℃时,反应平衡常数为 0.64,升高温度,平衡逆向移动,则正反应为放热反应,故C错误;
D.保持其他条件不变,起始时向容器中充入 0.60 molCO 和 1.20 molH2O,达到平衡时 ,设n(CO2)=x,由平衡常数= ,x=n(CO2)=0.4mol,故D正确;
,x=n(CO2)=0.4mol,故D正确;
故选D。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目