题目内容
11.以下各组均含有三种溶液,这三种溶液所含溶质的物质的量均相等,将它们充分混合后,不会产生沉淀的是( )| A. | AlCl3、Ba(OH)2、HCl | B. | BaCl2、Na2SO4、HCl | ||
| C. | MgCl2、NaOH、HNO3 | D. | NaAlO2、NaOH、H2SO4 |
分析 A.物质的量相等时,氯化氢能够消耗氢氧化钡溶液中一半的氢氧根离子,剩余的氢氧根离子与铝离子反应生成氢氧化铝沉淀;
B.氯化钡与硫酸钠溶液反应生成硫酸钡沉淀;
C.氢氧化钠与硝酸恰好发生中和反应生成硝酸钠和水,不会生成氢氧化镁沉淀;
D.氢氧化钠能够中和硫酸中一半的氢离子,剩余氢离子与偏铝酸钠反应生成氢氧化铝沉淀.
解答 解:A.AlCl3、Ba(OH)2、HCl,三者物质的量相等时,氢氧根离子不足,则铝离子与氢氧根离子反应生成氢氧化铝沉淀,故A错误;
B.BaCl2、Na2SO4发生反应生成硫酸钡沉淀,硫酸钡不溶于稀盐酸,故B错误;
C.等物质的量的NaOH、HNO3恰好发生中和反应,不会生成氢氧化镁沉淀,故C正确;
D.等物质的量的NaOH,H2SO4反应后氢离子有剩余,剩余氢离子与NaAlO2反应生成氢氧化铝沉淀,故D错误;
故选C.
点评 本题考查了离子反应发生条件,题目难度不大,试题侧重基础知识的考查,明确离子反应发生条件是解答关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
2.将碘酒滴到一片土豆上,可观察到土豆变蓝,说明土豆中含有( )
| A. | 醋酸 | B. | 淀粉 | C. | 葡萄糖 | D. | 纤维素 |
19.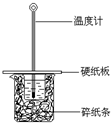 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法中,正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法中,正确的是( )
 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法中,正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法中,正确的是( )| A. | 实验过程中没有热量损失 | |
| B. | 图中实验装置缺少环形玻璃搅拌棒 | |
| C. | 烧杯间填满碎纸条的作用是固定小烧杯 | |
| D. | 若将盐酸体积改为60 mL,理论上所求中和热不相等 |
6.下列叙述正确的是( )
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 离子化合物中不可能含有共价键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 共价化合物中可能含有离子键 |
16.制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现
①Si(固)+3HCl(气)$\frac{\underline{\;300℃\;}}{\;}$ SiHCl3(气)+H2(气)
②SiHCl3+H2 $\frac{\underline{\;950℃\;}}{\;}$Si+3HCl
对上述两个反应的叙述中,错误的是( )
①Si(固)+3HCl(气)$\frac{\underline{\;300℃\;}}{\;}$ SiHCl3(气)+H2(气)
②SiHCl3+H2 $\frac{\underline{\;950℃\;}}{\;}$Si+3HCl
对上述两个反应的叙述中,错误的是( )
| A. | 两个反应都是置换反应 | B. | 据反应条件无法判断反应是否吸热 | ||
| C. | 两个反应互为可逆反应 | D. | 两个反应都是氧化还原反应 |
3.一表面已被氧化的金属钠,质量为10.8g,投入水中完全反应后,收集到H2的质量为0.2g,则被氧化的钠的质量为( )
| A. | 4.6g | B. | 6.2g | C. | 7.8g | D. | 9.2g |
20.某元素的阴离子Rn-,核外共有m个电子,又知R的质量数为A,则该元素原子里的中子数为( )
| A. | A-m-n | B. | A-m+n | C. | A-n+m | D. | A+n+m |
18.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1 mol CO2中含有原子数NA | |
| B. | 1 L 1mol/L的硫酸钠溶液中,所含Na+数为NA | |
| C. | 标准状况下,11.2 L水所含分子数为0.5 NA | |
| D. | 1 mol Fe和足量盐酸完全反应失去的电子数为2NA |